수분노화된 금속/KClO4 산화제 기반 고에너지 물질의 화학반응역학 변화를 유발하는 주요인자 확인
Copyright Ⓒ The Korean Society of Propulsion Engineers
This is an Open-Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License(http://creativecommons.org/licenses/by-nc/3.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
초록
고에너지 물질의 노화로 인하여 성능 감소를 최소화하기 위해 현재 노화 연구가 활발하게 진행되고 있지만, 개별 재료에 집중한 연구가 대부분이며 일반적인 노화 메커니즘 파악에는 미흡한 상태이다. 본 연구에서는 이러한 맹점을 해결하기 위해서 금속(W, Ti, Zr)과 KClO4 산화제를 기반으로 하는 고에너지 물질에 대하여 열/표면 분석을 수행하였으며, 이를 통해 고습도-고온 조건하에 노화된 해당 물질에서 보인 열역학적 특성 및 화학반응인자의 변화를 확인하였다. 그 결과, 금속 원소의 상태가 화학반응인자의 상당한 변화를 결정하였다. 즉, 금속의 산화 및 산화막 두께의 증가는 활성화에너지 평균값의 상승을 초래하였으며, 금속 원자의 전기음성도는 활성화에너지 값의 표준편차의 변화를 이끌어냈다.
Abstract
To minimize such loss due to aging, research on energetic materials is being actively conducted though, there are difficulties in identifying the comprehensive aging mechanisms as they focused on the respective materials. In this study, thermal and surface analysis were performed on energetic materials composed of metals(W, Ti, and Zr) and KClO4 oxidizer to solve the blind spots of this aging study. It was newly found that the metals in the hygrothermally aged compounds can cause significant changes in performance. For example, the growth in the thickness of the oxide film on the metals led to an increase in the average value of activation energy(Eα). In addition, the standard deviation of Eα tends to dependent on the type of metal, which is due to the difference in electronegativity.
Keywords:
Pyrotechnics, Hygrothermal Aging, Thermal Analysis, Accelerated Aging, Thermodynamic Characteristics키워드:
파이로지연제, 수분노화, 열분석, 가속노화, 열화학적특성1. 서 론
노화는 모든 물질이 겪게 되는 일반적인 반응이며 이에 따라 노화로 인하여 발생하는 성능감소는 피할 수 없는 문제라고 할 수 있다. 시간이 흐름에 따라 복합화합물 내에서 느린 속도로 복잡한 물리화학적 반응이 일어나게 되는데, 특히 금속 성분인 연료와 산화제, 바인더 등으로 구성된 고에너지 물질의 경우 노화로 인하여 금속의 산화, 산화제의 분해, 바인더의 열화와 같은 화학적 변화가 발생하여 성능감소를 겪을 수 있다고 알려져 있다[1-7]. 이때 높은 에너지 밀도를 보유하고 있는 고에너지 물질의 경우에는 설계 성능의 보존과 공정 및 보관과정에 있어서 우발적인 이슈 발생을 방지하기 위해 노화 문제에 더욱 집중을 필요로 하고 있다.
추진 시스템에 활용되는 고에너지 물질을 이루는 주요 구성성분은 앞서 언급하였듯이 금속연료와 산화제를 들 수 있으며, 이 두 성분 간에 일어나는 연소반응을 통해 발생하는 열 방출이나 압력을 통해 주어진 임무 요건을 실현할 수 있다. 특히 산화제에 있어서는 과염소산칼륨인 KClO4가 항공우주 고체 추진시스템에서 흔히 활용되는 대표적인 산화제라고 할 수 있다. 한편, 연료로 활용되는 금속성분은 종류에 따라 반응성과 발열 특성이 좌우되기 때문에 추진시스템의 용도에 따라서 다양하게 투입되고 있다.
현재까지 고에너지 물질에 대한 노화 연구로는 일반적인 노화 효과의 식별보다는 개별 물질에 집중하여 노화 연구가 진행되어왔다. 예를 들어 RDX와 HMX와 같은 고폭약 물질[8,9] 혹은 붕소[8], 실리콘[10], 알루미늄[11], 지르코늄[2]과 같은 금속연료 기반의 추진제, 파이로테크닉[1,3-5,12,13], 순수 금속/합금(e.g. bimetal thermite powders (Al/Fe2O3)[14], magnesium alloys[15], and Al-Mg-Si alloys[16])과 같이 대개 한 가지 물질에 해당하는 고에너지 물질에 집중하여 노화 연구가 진행되어왔음을 확인해볼 수 있다. 그런데 이러한 연구의 경우 조성 및 성분이 바뀌게 되면 제시된 노화 패턴을 다른 고에너지 물질에 적용하기 어렵다는 단점을 가지고 있다.
그리고 앞서 언급한 연구의 경우 고에너지 물질에 대하여 노화가 유발하는 열역학적 특성의 변화를 밝히기 위해서 대부분 differential scanning calorimetry(DSC)와 thermogravimetry analysis(TGA)를 활용한 열분석이 주로 수행되었다[1-5,7-10,12-16]. 뿐만 아니라, 이렇게 얻은 실험 결과들을 바탕으로 몇몇 연구들은 노화가 고에너지 물질의 연소반응에 일으키는 변화를 수치해석 기법을 적용하여 예측한 바 있으며[9,11], 한편 열분석 실험과 더불어 실제 연소실험을 통해 노화된 고에너지물질에 대하여 압력 조건에 따른 연소속도의 변화나 연소 지연 시간을 측정하는 연구가 진행되기도 하였다[11,13]. 열분석 이외에도 고에너지 물질 입자 간의 결합에너지, 형태학적 특성, 결정구조 등의 특징들을 X-ray photoelectron spectroscopy(XPS)[1,2,4,5,13], scanning electron microscope energy dispersive X-ray spectrometer(SEM-EDS)[3,5,11-14], X-ray diffraction(XRD)[3,4,14]를 활용하여 밝히기도 하였다. 해당 연구를 통해서 금속과 고체 산화제로 구성된 고에너지 물질의 경우, 일반적인 노화 효과로 1. 금속의 산화와 2. 산화제의 분해 현상이 나타남을 대표적인 노화 효과의 결과로써 확인해볼 수 있었다.
이처럼 금속과 고체 산화제로 구성된 고에너지 물질의 경우 금속의 산화와 산화제의 분해라는 일반적인 노화 효과가 밝혀진 바 있다. 하지만, 연료 및 산화제의 비율 혹은 금속의 종류와 같이 물질 내부의 시료 조성이 금속의 산화와 산화제 성분의 분해반응에 대하여 경향성을 가지며 정량적인 변화로 이어지는지는 아직 명확하게 파악되지 않았다. 따라서 개별적인 고에너지 물질에 대한 노화 분석은 노화로 인한 성능 열화의 일부 단서를 제공해줄 수는 있어도, 고에너지 물질의 근본적인 노화 모델을 구축하는 데에 있어서는 데이터가 불충분하다고 할 수 있다. 따라서 본 연구에서는 개별 고에너지 물질이 아닌 확장된 형태로써, 다양한 금속과 KClO4 산화제로 구성된 고체상태의 고에너지 물질의 노화 메커니즘을 열분석 및 표면분석 실험을 통해 자세히 밝히고자 하였다.
이러한 결과들은 개별 고에너지 물질 뿐만 아니라 금속 및 KClO4 산화제를 바탕으로 하는 다양한 물질로까지 확장하여 노화에 따른 성능변화의 종합적인 추세를 예상해볼 수 있을 것이다. 본 연구에서는 먼저 텅스텐 금속을 연료로 하는 텅스텐 파이로 지연제에 대하여 DSC-TGA 열분석을 수행하였으며, 노화로 인하여 나타나는 열 거동의 변화를 먼저 파악하고 이를 바탕으로 프리드만 등 전환법[17,18]을 적용하여 화학반응인자를 추출하여 이에 대한 노화 효과를 확인해볼 수 있었다.
그뿐만 아니라, 추출한 화학반응인자 결과 분석을 통계적으로 접근하여 반응역학에 대한 노화 효과를 평균값 및 표준편차라는 두 종류의 주요 인자에 따라 정량적인 관계를 밝혀내었다. 그리고 텅스텐뿐만 아니라, 티타늄 및 지르코늄을 연료로 하고 KClO4를 산화제로 사용하고 있는 THPP 개시제[1,5], ZPP 추진제[2]에 대해서도 화학반응인자를 추출하였으며 이를 노화 조건별로 비교하여 금속 종류와 그에 따라 변화된 화학인자의 상관관계를 도출하고자 하였다.
2. 실 험
2.1 실험 물질 및 노화 조건
본 연구에서는 텅스텐을 연료로 하는 텅스텐 파이로 지연제, 티타늄을 연료로 하는 THPP, 지르코늄을 연료로 하는 ZPP 즉, 총 세 종류의 파이로테크닉 물질을 다뤘다. Table 1에는 세 종류 파이로 물질에 대한 노화 조건과 함께 각 시료에 대한 명칭이 작성되어있다. 이때, 세 종류의 시료를 명확하게 구분하기 위해서 텅스텐 지연제는 ‘W’, THPP는 ‘T’, ZPP는 ‘Z’로 명명하였으며, 각 알파벳 단어 뒤에는 노화 주차를 표기하여 노화 시료 간의 비교를 더욱 쉽게 하고자 하였다.
물질 조성의 경우, 텅스텐 파이로 지연제는 질량 기준 48%의 W, 10%의 KClO4, 36%의 BaCrO4, 5%의 SiO2, 1%의 Rareox #14(Binder)로 구성되어있다. THPP는 30%의 TiH2, 65%의 KClO4, 5%의 Viton-b(Binder)로 구성이 되어있으며, ZPP는 52%의 Zr, 42%의 KClO4, 5%의 Viton-b(Binder), 1%의 흑연으로 이루어져 있다. 각 시료는 실험을 수행하기 전에 200 mesh sieve를 사용하여 입자의 크기를 75 μm 이하로 유지하여 입자 크기의 영향이 열분석 결과에 최소한의 영향을 미치도록 전처리를 수행하였다.
이때, 고에너지 물질의 경우 항공우주산업 표준[19]에 따르면, 71℃ 온도 조건으로 한 달 이상 보관되었을 때 시료 내에 특별한 열화 반응이 관찰되지 않을 경우에는 적어도 3년 이상의 기대수명을 보장할 수 있다고 알려져 있다. 노화의 경우, 시료마다 상대습도 조건과 최대노화기간에 있어 약간의 차이를 보이고 있지만, 공통으로 온도는 71℃로 고정한 상태에서 한 달 이상의 충분한 노화 기간을 가지게 하여 노화 효과를 더욱 정확하게 파악하고자 하였다. 그리고 상대습도의 경 70% 이상의 조건에서 노화된 시료를 다룸으로써 고습도 조건이 전이금속을 연료로 하고 KClO4를 산화제로 다루는 파이로 물질의 열역학적 특성에 끼치는 수분노화효과를 확인해보고자 하였다.
노화 시료 중에서 THPP가 가장 고습도인 100% RH에서 노화되었으며, 그다음으로는 텅스텐 파이로 지연제가 95% RH 조건에서 보관되었다. 마지막으로 ZPP가 가장 낮은 습도라고 할 수 있는 70% RH 조건에서 노화되었다. 노화 기법의 경우, 텅스텐 파이로 지연제는 수증기 및 온도 조절이 가능한 챔버 내에서 보관하는 방식으로 노화가 이루어졌다. THPP와 ZPP의 경우, 71℃ 온도 조건에 해당하는 수증기압과 이상기체법칙을 적용하여 4.7 L 부피의 밀폐 용기 내에 정제수의 양을 조절함으로써 상대습도 조건을 맞추었으며, 이를 71℃로 설정된 건조 오븐 내에 일정 기간 보관하는 방식으로 노화를 진행하였다.
이때 71℃에 해당하는 온도 조건은 고에너지 물질에 대한 American Institute of Aeronautics and Astronautics(AIAA)의 항공우주 및 발사체의 폭발 시스템 및 장치에 대한 기준[19]을 따랐다.
2.2 열분석 실험
열분석 실험의 경우 Mettler Toledo 사의 시차주사 열량계인 DSC 3+ 기기와 열중량 분석기인 TGA 2 기기를 사용하였다. 텅스텐 파이로 지연제의 경우, DSC 실험에서는 약 2∼4 mg의 분말을 열분석용 40 μL 표준 알루미늄 샘플 팬에 담아 실험에 투입하였다. 이때, 팬 내부에 자기가열효과 발생을 미연에 방지하기 위해 샘플 팬 뚜껑 중앙에 0.1 mm 지름의 구멍을 뚫어 팬에 봉한 후, 샘플팬을 최종적으로 가열로에 투입되도록 하였다. DSC 실험 수행에 있어 온도 조건은 30℃에서 600℃까지 1, 2, 4, 8℃/min의 네 개의 다른 승온속도 조건에서 가열되도록 설정하였다. 이때, 600℃ 이하의 온도 조건의 경우 연료인 W과 산화제 중 하나인 KClO4 간의 반응이 이루어지고, 그 이상의 온도 영역 대(1,400 K 이상)에서는 시료 내에 또 다른 산화제인 BaCrO4와 W 사이의 화학반응이 발생한다고 알려져 있다. 본 연구에서는 전이 금속과 KClO4의 반응에 대한 수분노화효과 분석에 집중하였기 때문에 W 및 BaCrO4간의 연소반응은 고려하지 않았다.
한편, TGA 실험의 경우에는 약 5 mg에 해당하는 분말을 열분석용 70 μL 표준 세라믹 샘플 팬에 투입하여 실험이 진행되었다. 온도 조건의 경우 10℃/min의 단일 승온속도 조건에서 30℃∼900℃까지 가열시켜 해당 온도 범위 내에서 발생하는 산화 및 분해반응을 확인하고자 하였다.
열분석 실험을 수행하는 데 있어 반복성 입증을 위해 실험 케이스당 2회 이상의 실험을 진행하였으며, 국제 열분석 및 열량측정 위원회(The International Confederation for Thermal Analysis and Calorimetry(ICTAC) Kinetics Committee)[18]의 권고사항을 따라 정확한 실험 결과를 도출해낼 수 있도록 노력하였다.
2.3 화학반응인자 계산 기법
다섯 가지의 다른 승온속도에서 수행한 DSC 실험 결과를 바탕으로 Eq. 1∼Eq. 4에서와 같이 프리드만 등 전환법[17,18]을 적용하여 각 노화 시료에 대한 화학반응인자를 추출할 수 있었다.
| (1) |
| (2) |
| (3) |
| (4) |
위 식에서 Q, t, t0, tend, S(t), B(t)는 각각 발열량(J/g), 시간(s), 발열반응 개시 시점, 발열반응 종료 시점, DSC 데이터, 베이스라인 데이터를 의미한다. 또한, Eq. 2∼Eq. 4에서 나타나 있는 α, β, Eα, Aα, R, T는 반응률, 승온속도(K/min), 활성화에너지(kJ/mol), 빈도인자(1/s), 이상기체상수(J/molK), 온도(K)를 나타낸다.
DSC 실험 결과를 바탕으로, 나타난 발열반응 구간에 대하여 시간에 대해 적분하면, 발열량 Q를 계산할 수 있게 된다. 이 발열량 값에 기반하여 반응률 α가 정의되며, 승온속도가 곱해진 반응속도와 아레니우스 기반의 반응속도를 각각 좌 우변에 두면 시료에 대한 화학반응인자 계산이 가능해진다. Eq. 4에서 나타난 아래첨자 α와 i의 경우 각 반응률 및 승온속도에 대한 값을 의미하며, 이는 다른 승온속도 조건에서 수행된 실험값을 바탕으로 전환율이 동일한 점들에 대하여 일차함수를 구하여 화학반응인자를 추출할 수 있음을 보여준다. 다시 말해서, x축을 온도의 역수로 y축을 ln(β*(dα/dT))로 설정하였을 때 기울기를 통해 활성화에너지를 얻을 수 있고, y절편을 통해 빈도인자를 얻을 수 있다는 것이다.
3. 실험 결과
3.1 시차 주사 열량측정 결과
Fig. 1에서는 DSC와 TGA를 통해 얻은 텅스텐 파이로 지연제 시료에 대한 열분석 실험 결과들을 보여주고 있다. Fig. 1(a)에서는 노화되지 않은 텅스텐 파이로 지연제에 대하여 네 가지의 다른 승온속도에서 수행한 DSC 실험 결과를 보여주고 있다. 결과에서 나타난 바와 같이 승온속도가 높아질수록 그에 해당하는 DSC 결과 또한 높은 온도로 이동하는 경향을 보였는데, 이는 발열반응이 운동학적 프로세스로 진행되는 비가역 과정임을 의미한다.
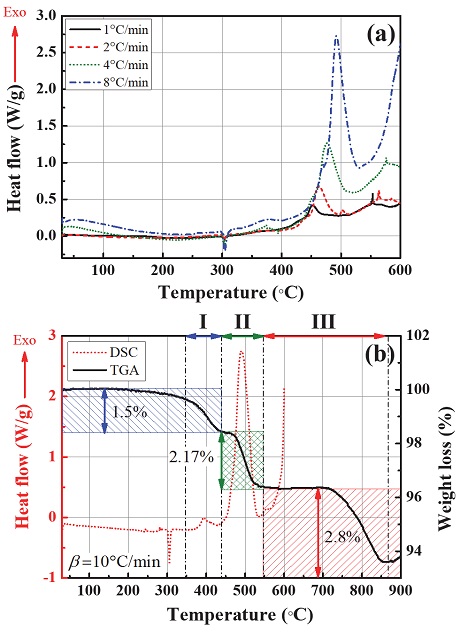
(a) DSC profiles of #W0 at four-different heating rate conditions and (b) DSC-TGA results for #W0 at 10℃/min.
Fig. 1(b)에서는 10℃/min 조건에서 얻은 DSC와 TGA 실험 결과를 동시에 보여주고 있다. 먼저 DSC 결과를 확인해보면, 텅스텐 파이로 지연제가 다양한 조성으로 이루어져 있기 때문에 이에 따라 나타난 시료 열 거동 반응 또한 다소 복잡하게 이루어져 있음을 알 수 있다. 우선 300℃ 부근에서 흡열반응이 나타났는데, 이는 산화제인 KClO4의 상변화 과정[20]을 의미한다. 곧이어 총 세 가지의 발열반응이 확인되었다. 먼저 약 380℃ 근처에서는 작은 발열반응(I)이 나타났으며, 이는 바인더 역할을 하는 Rareox #14의 산소 환원 과정[21] 및 분해반응으로 인하여 비롯된 현상이라고 할 수 있다. 그뿐만 아니라, 텅스텐의 사전 산화 반응[3]도 관여되어있을 것으로 추정된다. 이어서 보인 주 발열반응(II)은 약 400℃에서 시작되었으며, 산화제인 KClO4 및 잔여 바인더의 분해반응과 텅스텐의 산화반응으로 여겨진다[20]. 뿐만 아니라, 500℃ 이후에서도 W, KClO4, BaCrO4간의 연소반응[20]을 의미하는 세 번째 발열반응 (III)이 나타났는데, 본 연구에서는 텅스텐과 KClO4간의 반응만 고려하기 때문에 해당 발열반응은 분석에서 제외되었다.
한편, TGA 데이터에서는 DSC에서 확인된 발열반응 과정에 상응하여 무게가 감소하는 결과를 보였다. 먼저 100℃ 이후에서 수증기의 증발현상이 천천히 나타나다가 350℃에서부터 무게가 약 1%가량 감소하였는데, 이는 시료 조성에서 1%를 차지하고 있는 바인더인 Rareox #14의 분해반응을 의미한다. 이어서 약 440℃에서 550℃ 범위에서 약 2.17%의 추가적인 무게 감소 현상이 나타났다. 이는 KClO4의 분해반응으로 인하여 나타나는 결과라고 할 수 있다. 그리고 마지막으로 세 번째 발열반응에 해당하는 온도영역에서 무게 감소가 확인되었는데, 이는 또 다른 산화제인 BaCrO4의 분해 현상에 기인한 것으로 볼 수 있다.
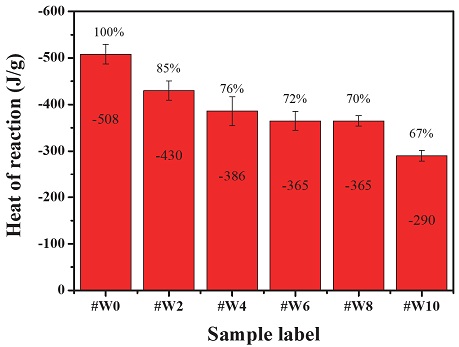
노화된 텅스텐 파이로 지연제에 대한 DSC 결과를 바탕으로 발열량을 계산해본 결과, Fig. 2와 같은 발열량 변화를 파악해볼 수 있었다. 먼저 노화되지 않은 텅스텐 파이로 지연제(#W0)의 경우, -508±21 J/g의 발열량을 보유하고 있었으며, 이전에 Lu et al.[20]을 통해 발표되었던 텅스텐 파이로 지연제의 발열량 값인 –341.6±10.2 J/g[20]와 비교해보았을 때 약 1.5배가량 높은 수치를 가졌다. 이러한 차이는 화합물 내 조성 차이에서 비롯된 것으로 추정되는데, Lu et al.[20]의 경우 전체 함량 중 텅스텐의 비율이 33%이지만 본 연구에서는 48%로 약 15% 증가한 함량을 갖기 때문이다. 텅스텐 산화반응의 경우 텅스텐과 산소 기체가 각각 2 mol(W)과 3 mol(O2)의 화학양론계수를 가질 때, 이상적인 산화반응을 진행할 수 있게 된다. 본 연구에서 다루는 텅스텐 파이로 지연제는 연료 과잉 조건에 해당하는 조성을 가진 관계로, 발열량이 다소 높게 측정된 것으로 추정된다.
한편, 수분 노화 된 시료들의 결과를 보면 노화 주차가 길어질수록 발열량 데이터도 감소하는 추세를 보였다. 이때, 노화 4주차까지는 노화가 2주 동안 진행될 때마다 평균 발열량 값이 9∼15%가량 발열량 성능이 크게 하락하는 반면, 노화 주차 4주에서 8주차까지는 2∼4%의 낮은 수치로 감소하는 결과를 보였다. 이러한 현상은 노화된 시료 내에 금속과 반응하지 못하고 남아있던 산화제 성분이 분해되면서 발생하는 발열량으로 인한 상쇄 효과로 설명이 가능하다. 이는 수분 노화가 텅스텐 파이로 지연제 시료내부에서 텅스텐으로부터 산화 텅스텐(WO3)의 생성을 유발할 수 있음을 보여준다.
그뿐만 아니라, #W10의 경우 약 33%가량 감소한 발열량 성능을 보여 텅스텐 파이로 지연제가 수분 환경에 취약한 특성을 가지고 있음을 보여주고 있다.
3.2 피크 분리 기법을 적용한 노화효과 확인
수분 노화 된 텅스텐 파이로 지연제 시료의 경우, 더욱 자세한 열 거동 분석을 위해 DSC 실험(8℃/min 조건)으로부터 얻은 반응속도 데이터에 피크 분리 기법을 적용하였다. Fig. 3에서 본 연구에서 사용된 비노화 및 노화된 텅스텐 파이로 지연제 시료에 대한 결과들을 확인해볼 수 있다.
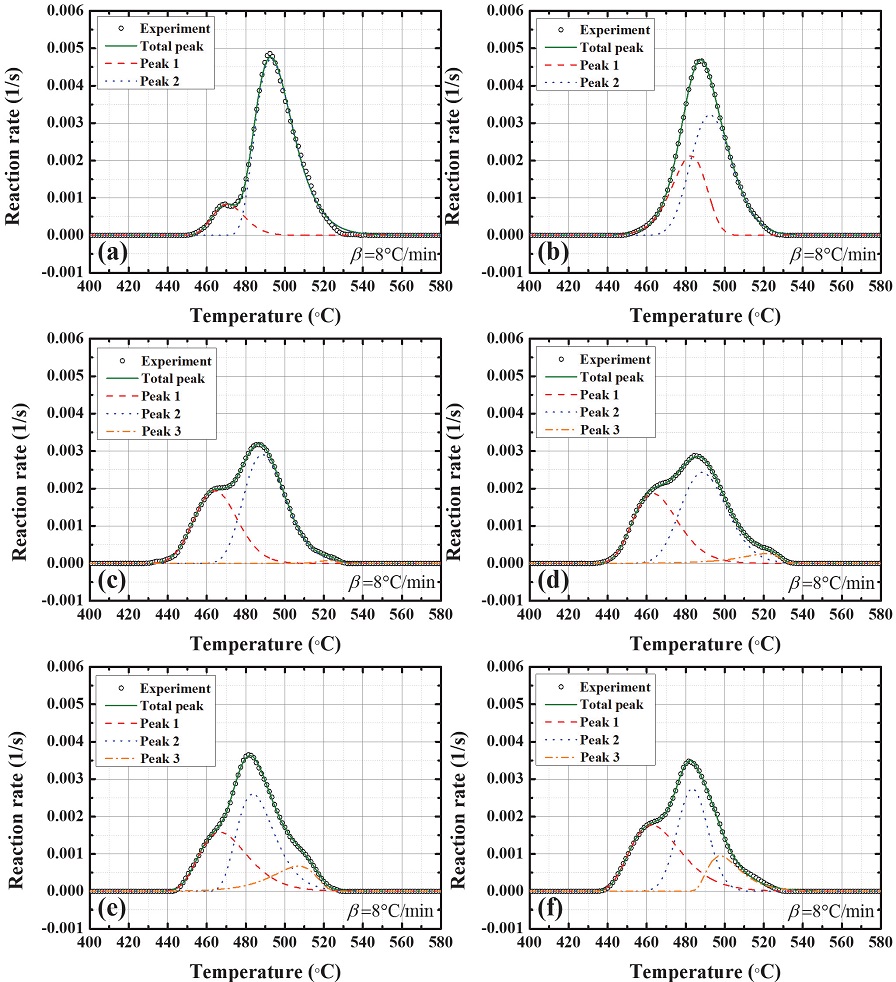
Observed sub-peak by applying the peak deconvolution method to the DSC signals. (a) #W0, (b) #W2, (c) #W4, (d) #W6, (e) #W8, and (f) #W10.
먼저, Fig. 3(a)에서는 노화되지 않은 시료인 #W0의 발열반응을 구성하고 있는 하위 발열반응들을 보여주고 있다. 약 450∼500℃ 범위에서 나타난 Peak #1은 바인더의 분해반응을 의미하며, 그 이후인 470∼540℃에서 보이는 발열반응인 Peak #2는 텅스텐과 KClO4간의 화학반응을 나타낸다.
이때, 수분 노화 된 시료에서는 #W0과 다른 양상이 나타나는 것을 확인해볼 수 있었다. 단기간 노화된 시료인 #W2를 제외한 모든 시료에서 약 520℃ 부근에서 새로운 발열반응인 Peak #3가 나타났는데, 해당 반응은 연료인 텅스텐과 반응하지 못하고 남아있던 KClO4의 분해반응을 의미한다. 이는 앞서 Fig. 2에서 제시된 수분 노화 시료의 발열량 감소와 상응하는 결과로, 산화 텅스텐의 함량이 수분노화로 인하여 증가하기 때문에 연료와 반응하지 못하는 산화제가 발생하게 되는 것이라고 할 수 있다. 그리고 노화 주차 6주 이상부터 잔여 산화제의 분해반응은 두드러지게 증가하는 경향을 보였으며, 이는 오래된 노화 주차에서 잔여 KClO4의 함량이 늘어났음을 의미한다. 한편, 바인더 분해반응을 나타내는 Peak #1은 수분 노화 시료의 경우 #W0의 결과와 비교해보았을 때 상대적으로 반응속도가 약 2배 정도 증가하는 추세를 보였다. 이러한 현상은 수분노화효과 중 하나로 산화제인 KClO4가 KClO3로 사전 분해되는 반응에 기인하는 결과라고 할 수 있다. KClO3의 경우 KClO4보다 높은 반응성을 가지고 있기 때문에 KClO4보다 더 낮은 온도 범위에서 KCl과 O2로 분해반응을 진행할 수 있다. 따라서 Fig. 3(b-f)에서는 바인더의 분해반응에 KClO3의 분해반응이 겹쳐 나타나 반응속도가 증가하는 것처럼 보이는 결과가 나타나게 된 것이라고 해석해볼 수 있다. 그뿐만 아니라, 수분 노화 된 텅스텐 파이로 지연제의 경우 주 발열반응이라고 할 수 있는 텅스텐 산화반응인 Peak #2에서 상당한 열화를 보였다. 예를 들어, 온도 범위의 경우 #W0는 470∼540℃에서 Peak #2가 나타났지만 #W10에서는 460∼500℃로 상당히 좁아진 온도 범위에서 Peak #2가 나타났다. 그럴 뿐만 아니라 반응속도 측면에서는 #W0는 0.0050/s의 최댓값을 가졌지만 #W6 또는 #W8에서는 절반가량 줄어든 0.0025/s의 최댓값이 확인되었다. 이러한 현상은 노화가 오래 진행될수록 두드러지게 나타났으며, 종합해보자면 수분 환경이 텅스텐 파이로 지연제의 조성에 있어서 텅스텐의 산화, KClO4 산화제의 사전 분해 및 잔여 KClO4의 생성과 같은 결과를 초래할 수 있다고 정리해볼 수 있다.
3.3 텅스텐 파이로테크닉 지연제의 화학반응인자 분석
본 연구에서는 1, 2, 4, 8℃/min에서 수행된 네 가지의 다른 승온속도에서 수행된 DSC 실험 데이터를 바탕으로 프리드만 등 전환법을 적용하여 Fig. 4와 같이 반응률에 따른 활성화에너지 (Fig. 4(a))와 빈도인자(Fig. 4(b)) 즉, 화학반응인자를 추출할 수 있었다. 나타난 화학반응인자는 440∼540℃ 범위에서 확인된 W 및 KClO4 반응에 해당하는 발열반응에 대하여 추출한 결과이며, 반응률에 따라 총 다섯 가지 단계(I, II, III, IV, V)로 구분 지을 수 있었다.
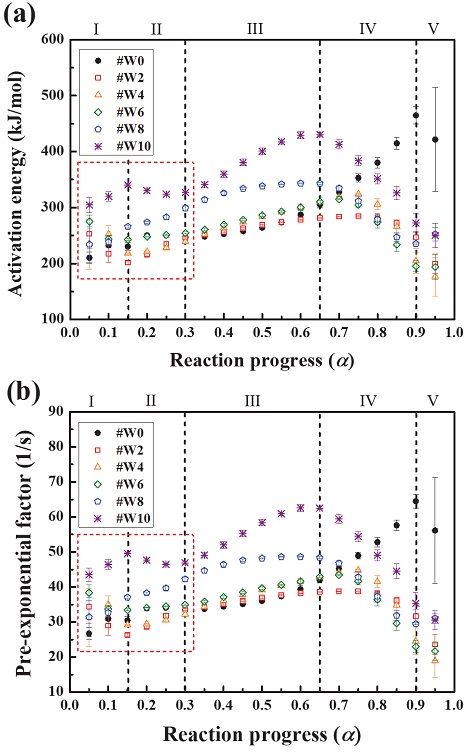
Calculated chemical reaction kinetics of the utilized W delay pyrotechnic samples. (a) Activation energy and (b) pre-exponential factor.
먼저, 반응개시단계(I)와 반응종결단계(V)에서는 데이터의 불안정성 및 적분 접선형 방식의 베이스라인 설정 시 데이터마다 기울기가 상이하기 때문에 다른 구간에서 나타난 것보다 편차가 큰 결과를 보였다. 그뿐만 아니라 반응이 시작되는 단계에서는 물질 고유의 화학반응인자가 완전히 반응속도가 결정되지 않은 상태이기 때문에, 보통 해석을 진행하는 데 있어 배제되는 경우도 있다. 따라서 본 연구에서도 화학반응인자 해석에 있어서 반응이 약 15%에서 90%까지 진행되었을 때 해당하는 반응인 II, III, IV에 집중하였다. 이때, 위 세 반응은 다음과 같이 정의된다.
- ● II. 바인더의 분해반응
- ● III. W과 KClO4간의 연소반응
- ● IV. W과 KClO4간의 연소반응 및 잔여 KClO4의 분해반응
우선, 비노화 시료인 #W0의 경우 II∼IV 구간에서 전반적으로 증가하는 추세를 보였다. 이러한 화학반응인자의 연속적인 증가는 독립적인 화학반응이 병렬적으로 발생하여 나타난 결과라고 설명이 가능하다. 이때, IV 구간에서 특히 #W0의 화학반응인자가 급격히 상승하는 결과를 보였는데, 이는 IV 구간에서 각기 다른 반응속도를 가진 다양한 반응들이 개별적으로 영향을 미치며 이러한 반응들이 결국에는 전체적인 파라미터의 증가로 이어지게 됨을 나타낸다. 그중에서 W와 KClO4간의 연소반응이 IV 구간 후반부의 화학반응인자 결정 단계에서 상당한 변화를 가져올 수 있는 주요 반응이기 때문에, 해당 반응이 반응률에 따른 화학반응인자 기울기의 급격한 증가의 가장 큰 원인으로 작용함을 추정해볼 수 있다.
한편, 수분 노화 된 텅스텐 파이로 지연제의 경우 구간 II와 구간 III에서는 #W0 값과 비교했을 때 대체로 더 큰 값을 가졌다. 특히, 10주간 노화된 시료인 #W10의 경우 약 1.5배가량 더 증가했음을 확인해볼 수 있었다. 이렇게 II 및 III 구간에서 관찰된 활성화에너지의 상승은 연료인 텅스텐 금속 표면의 산화막 형성에 기인하는 결과라고 할 수 있다. 금속 표면의 산화막 성장은 텅스텐 금속과 산소 기체와의 산화 반응을 차단할 수 있기 때문이다[3,5,13,22]. 이와 더불어 노화로 인하여 형성된 금속 표면에 위치한 산화막 (MgO)은 금속 이온(Mg2+)의 이동을 더욱 쉽게 만들어 산화막 내부 및 외부에서의 확산현상을 강화해 결국에는 표면의 균열현상을 초래할 수 있다고 알려져 있다[3,5,13,22]. 그리고 노화 시료 사이에서도 노화 주차에 비례하여 화학반응인자의 값이 증가하는 경향성이 나타났다. 이러한 결과는 또한 금속 표면의 산화막 성장으로 설명이 가능하다. 노화 기간이 오래될수록 텅스텐 파이로 지연제는 외부 수분 환경에 더 오래 노출이 되기 때문에, 노화 기간이라는 독립변인이 산화막 두께라는 종속변인의 증가를 초래하게 된다.
그리고 II 구간에서는 수분 노화 된 시료들이 반응을 진행할 때 약간의 변동성을 보였지만, III 구간에서는 대체로 단조 증가하는 형태가 확인되었다. 그리고 노화 시료들의 경우 IV 구간에서는 오목하게 증가하는 #W0과는 다르게, 반응이 약 65%가량 진행되었을 때 최댓값을 가지면서 볼록한 형태로 감소하는 결과를 확인해볼 수 있었다. 이는 수분 노화 된 시료의 경우, III 구간에서 병렬적으로 발생했던 다양한 반응들이 IV 구간으로 이동할 때, 고체에서 기체로의 확산반응이 지배적으로 나타났음을 보여주는 결과라고 할 수 있다. 이는 이전의 피크 분리 기법을 통해 확인했던 것과 상응하는 결과라고 할 수 있다. 바로 수분 노화 된 시료의 연소반응에서 반응하지 못한 채로 남아있던 고체상태의 잔여 KClO4가 산소기체로 분해되는 현상이 두드러지게 나타났는데, 이러한 현상으로 인하여 IV 구간에서 노화 시료의 상이한 특성이 발현하게 된 것이다.
4. 전이금속과 KClO4 산화제 기반의 파이로테크닉 물질에 대한 일반적인 노화 효과
4.1 화학적 조성 변화
본 연구에서 다루는 물질인 ‘텅스텐 파이로 지연제’와 ‘THPP’, ‘ZPP’는 연료는 전이 금속에 해당하는 ‘W’, ‘Ti’, ‘Zr’이며, 산화제로는 고체 분말 형태의 KClO4를 활용한다는 공통점을 가지고 있다. 이러한 사항을 바탕으로 세 종류의 파이로 물질이 고습도 환경에 노출되어 수분 노화가 되었을 때, 화학적 조성 측면에서 어떠한 특징적인 결과를 보이는지 확인해보고자 하였다.
Fig. 5(a)와 5(b)는 각각 THPP에 포함된 연료 성분인 Ti 원소에 대한 화학적 변화와 산화제 성분인 Cl 원소에 대한 화학적 변화를 보여주고 있다. 이와 마찬가지로 ZPP의 경우에서도 연료 성분인 Zr 원소에 대한 화학적 변화(Fig. 5(c))와 산화제 성분인 Cl 원소에 대한 화학적 변화(Fig. 5(d))를 찾아볼 수 있다. 결과를 통해 확인해볼 수 있듯이 THPP와 ZPP모두 수분 노화 된 시료에서 연료의 산화 현상이 심화되었다. 다만 그 심화되는 정도는 금속에 따라 차이를 보였는데, THPP의 경우 노화 8주차(#T8)까지는 TiO2의 피크가 점진적으로 증가하다가 노화 주차가 16주차(#T16)에 다다르자 신호가 급격하게 증가하는 결과가 나타났다. 그뿐만 아니라, Fig. 5(b)에서 나타나 있듯이 KClO4에 해당하는 신호도 #T16에서 급격하게 감소하여 노화 16주차 이상에서 산화제 분해 현상이 두드러지게 발생하였음을 추정해볼 수 있다. 반면 ZPP의 경우 노화 2주차부터 산화제 분해 현상이 두드러졌으며, 연료의 사전산화의 경우 노화 4주차에서 뚜렷하게 나타났다.
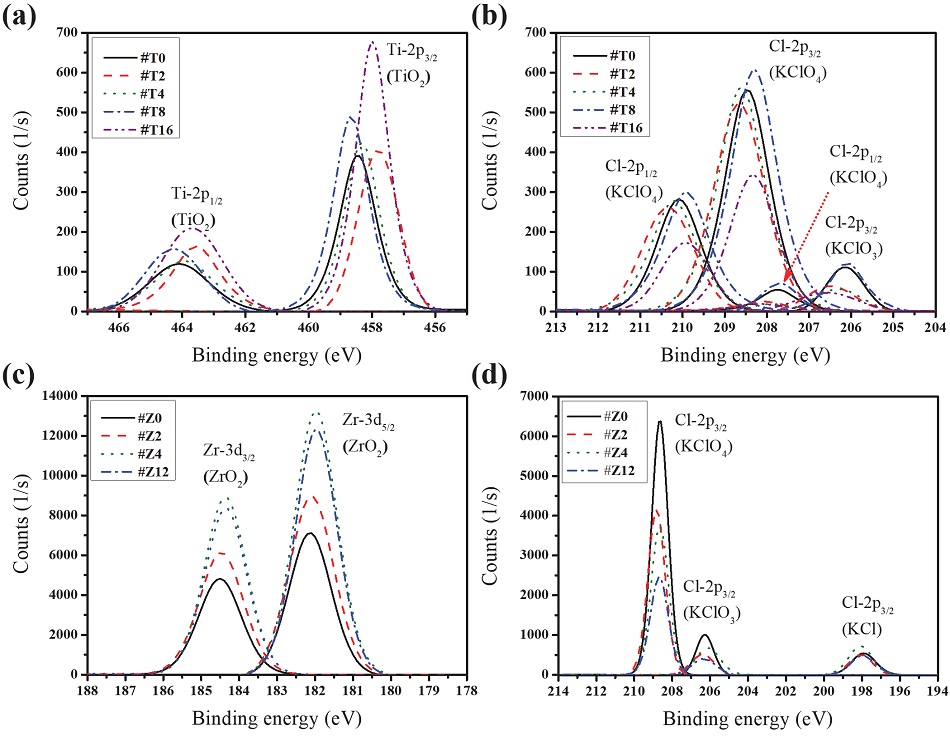
XPS spectra for (a) Ti2p (TiH2 in THPP), (b) Cl 2p (KClO4 in THPP), (c) Zr 3d (Zr in ZPP), and (d) Cl 2p (KClO4 in ZPP).
이렇게 파이로 물질에서 주요하게 발생한 두 가지 노화 효과 즉, 1. KClO4 산화제의 사전 분해와 2. 금속의 사전산화는 이전에 진행되었던 텅스텐 파이로 지연제 노화 연구에서 파악된 결과[3]와 상응하는 결과라고 볼 수 있다. 이러한 공통적인 변화가 나타난 원인을 고려해보면, KClO4 산화제의 결합세기를 들 수 있다. KClO4 산화제의 경우 고습도 환경에 노출되면 Cl-O의 약한 결합이 쉽게 끊어질 수 있기 때문에 수분 노화 효과로써 KClO4의 사전 분해를 야기하게 된다. 그런데 이 과정에서 KClO4 산화제로부터 분리되어 나온 산소 기체가 근접하게 위치한 금속 성분을 쉽게 환원시키는 역할을 수행하게 된다. 이는 최종적으로 전이 금속(i.e., W, Ti, Zr)의 다룬 파이로 물질 중에서는 수분 환경에 노출되었을 때 Ti 성분이 가장 산화에 견고한 특성을 보였다.
4.2 발열 성능 변화
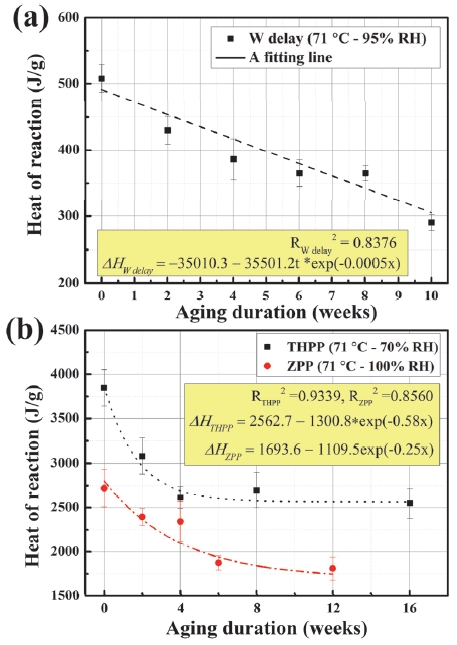
일반적으로 파이로 물질의 발열 성능은 연료와 산화제의 비율에 따라서 조절이 가능하다. 그런데 앞서 수분 노화가 파이로 물질 내부에서 금속의 산화와 산화제의 분해 현상을 발현시킬 수 있음을 확인하였다. 결과적으로 이는 화학적 조성 측면에서 연소 반응에 참여할 수 있는 연료와 산소의 비율을 변화시키게 된다. 본 연구에 서는 세 종류의 파이로 물질이 노화 주차에 따라 어떠한 발열량의 감소세를 보이는지 DSC 실험 데이터를 바탕으로 발열량을 계산해보았으며, 결과는 Fig. 6에 나타나 있다.
Fig. 6(a)의 경우 텅스텐 파이로 지연제에 대한 발열량 변화를 보여주고 있으며, Fig. 6(b)에서는 THPP와 ZPP에 대한 발열량 열화 경향을 동시에 도시하였다. 이때, 세 종류의 파이로 물질 모두 Eq. 5와 같이 지수 모델을 따르면서 감소하는 경향을 보였으며, 각 물질에 대한 열화 모델은 Table 2에 나타난 바와 같다.

Estimated heat degradation models for the utilized pyrotechnic materials that were hygrothermally aged.
모든 시료가 지수 모델을 따르긴 했지만, Table 2에 나타난 바와 같이 시료 종류에 따라 계수가 상이한 값을 가졌다. 예를 들어, 텅스텐 파이로 지연제의 경우 다른 두 시료와 비교했을 때 매우 높은 y0와 A의 값을 가졌지만 R0의 값은 극히 작은 값을 가졌다. 이러한 차이는 주기율표상에 나타난 금속 사이의 족, 즉 원자가전자 수가 상이하기 때문에 나타난 결과라고 볼 수 있다. 예를 들어, 텅스텐의 경우 주기는 6이며 족은 6에 해당하는데, 티타늄과 지르코늄의 경우 같은 족인 4족에 속해있으며 주기는 4주기와 5주기로 다르다. 따라서 Fig. 6(b)에 나타난 바와 같이 THPP와 ZPP의 경우 동일한 원자가전자 수를 가져 비슷한 금속 특성을 공유하게 되고 이는 유사한 계수를 가진 열화 모델로 나타나게 된다. 이러한 결과를 통해, 금속의 반응성 및 주기적 특성이 화합물 내부에서 산화 금속의 생성량에 영향을 끼칠 수 있으며, 이는 최종적으로 발열량 열화를 결정짓는 주요한 요인이 될 수 있음을 보여준다.
| (5) |
4.3 화학반응인자 변화
Fig. 7에서는 DSC 실험 결과에 프리드만 등 전환법을 적용하여 추출한 텅스텐 파이로 지연제(Fig. 7(a)), THPP(Fig. 7(b)), ZPP(Fig. 7(c)) 각각에 대하여 반응률에 따른 활성화에너지 값에 대하여 각각 평균값과 표준편차를 추출하여 정규분포로 나타내었다. 이때, 세 종류의 파이로 물질 모두 통계적인 관점에서 활성화에너지 변화를 분석해보면, 노화 주차가 증가함에 따라 높은 활성화에너지로 이동하는 공통적인 현상을 보였다.
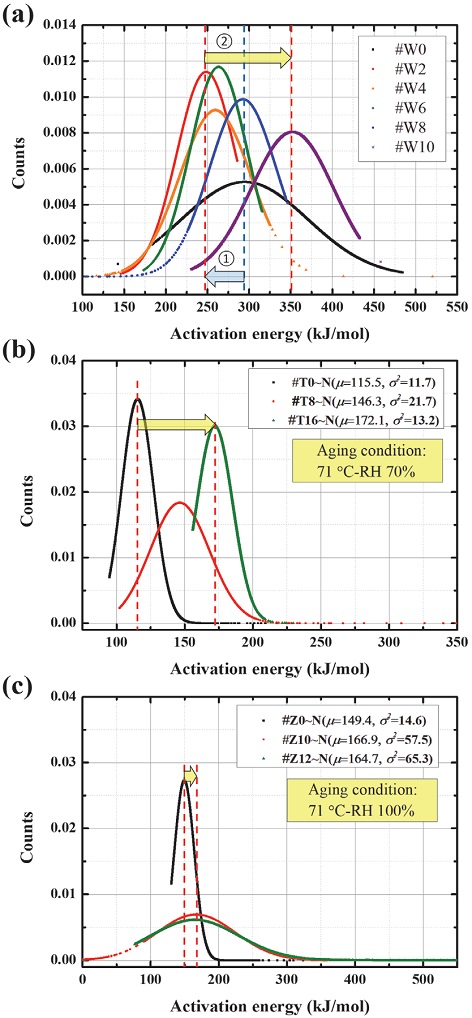
Activation energy values represented by Gaussian function. (a) W delay pyrotechnics, (b) THPP, and (c) ZPP.
먼저 텅스텐 파이로 지연제의 경우, 각 시료에 대한 활성화에너지의 정규분포 모델은 Fig. 7(a)에 나타나있으며, 평균값 및 표준편차와 같은 자세한 데이터 결과는 Table 3에서 확인이 가능하다. 먼저, 노화 2주차 시료인 #W2에서 활성화에너지의 평균값이 248.4 kJ/mol로 측정되어 294.7 kJ/mol의 평균값을 갖는 #W0에 비하여 약 15% 정도 작은 값을 보였지만, 그보다 더 오랜 기간 동안 노화되었을 때는 평균값이 점차 증가하는 추세가 확인되었다. 이렇게 노화 초반에 활성화에너지의 감소 현상이 나타난 원인으로는 앞서 열분석을 통하여 확인한 주요 노화 효과인 ‘KClO4 산화제의 사전 분해’와 ‘텅스텐 금속의 산화 현상’을 들 수 있다. 노화 초기에는 KClO4산화제 내부에서 비교적 결합세기가 약한 Cl-O 결합이 끊어지게 되어 산화제의 사전 분해 현상이 주요하게 이루어지게 된다. 이때 분해과정을 통해 생성된 KClO3분자는 KClO4보다 반응성이 좋아 연소반응에 요구되는 에너지 장벽이 다소 낮아지게 되는 효과가 나타난다. 그러나 수분 노화가 오랜 기간 동안 진행이 되면, 산화제 분해반응으로 인하여 방출된 산소의 영향력이 커지게 되고 텅스텐 금속 입자의 산화막 형성에 활발하게 기여하게 된다. 따라서 노화 기간이 오래될수록 텅스텐 금속의 산화 현상이 우세해지며, 이는 다시 말해 금속 입자 표면을 둘러싸고 있는 산화막 두께가 노화 주차에 비례하여 점차 두꺼워지고 그 양 또한 증가하게 됨을 의미한다. 따라서 텅스텐 금속 입자의 산화막 형성 및 산화막 두께 증가로 인한 반응성 저하 때문에 Fig. 7(a)과 같이 연소반응에 필요한 활성화에너지 증가하게 되는 결과를 가져오게 된다.
한편, THPP와 ZPP의 경우도 마찬가지로 Fig. 7(b)과 7(c)에 나타나 있듯이 노화 주차에 따른 활성화에너지의 증가추세가 확인되었다. 다만, 증가하는 정도는 물질에 따라 다소 차이를 보였다. 예를 들어, THPP의 경우 #T0의 경우 115.5 kJ/mol의 평균값을 가졌는데 #T16의 경우 약 50% 증가한 172.1 kJ/mol의 활성화에너지를 가졌다. ZPP의 경우 149.4 kJ/mol의 활성화에너지 값을 가지는 #Z0와 비교했을 때, 12주간 노화된 시료인 #Z12에서는 약 10%가량 증가한 164.7 kJ/mol의 값을 보여주었다. 10주간 노화된 텅스텐 파이로 지연제인 #W10이 #W0에 비하여 약 20% 증가한 활성화에너지 값을 가지는 사실을 비교해보았을 때, 티타늄이 포함된 고에너지 물질인 THPP가 수분 노화 되었을 때 가장 급격하게 증가하는 활성화에너지 값을 보여주어, 해당 고에너지 물질이 금속 성분의 사전 산화에 있어 가장 취약한 성질을 가짐을 확인해볼 수 있다.
한편, 제시된 Fig. 7에서 활성화에너지의 평균값뿐만 아니라 표준편차에 대해서도 조성에 따라 특정한 변화가 나타났다. 텅스텐 파이로 지연제의 경우 노화된 시료에서 표준편차의 감소가 공통으로 발견되었지만, THPP와 ZPP의 경우에는 노화된 시료에서는 증가한 표준편차를 가지는 정규분포 모델이 확인되었다.
각 화학반응의 경우 고유한 활성화에너지 값을 가지고 있는데, 반응물의 결합 또는 분해를 통해 새로운 생성물을 만들어낼 때 이 활성화에너지 값 이상의 에너지가 제공되어야 반응이 진행될 수 있다. 따라서 표준편차의 증감은 연소 반응할 때에 발생하는 중간 생성반응의 증감과 관련지어 해석해볼 수 있다. 예를 들어, 텅스텐 파이로 지연제의 경우, 노화가 가해졌을 때 활성화에너지의 정규분포가 낮은 표준편찻값을 가져 연소반응 진행 중에 발생하는 중간 생성반응이 감소하는 결과를 보여주지만 THPP와 ZPP의 경우는 이와 반대로 노화가 되었을 때 활성화에너지의 표준편차가 증가하여 연소 중에 발생하는 중간 생성반응이 늘어나는 현상이 나타났다.
이렇게 시료마다 활성화에너지의 표준편차 값이 상이한 이유는 물질 내 이루고 있는 금속 원자의 차이를 원인으로 들 수 있다. 각 원자의 경우 전기음성도라는 고유한 특성을 가지고 있는데, 이는 공유결합을 하는 원자가 전자를 자기 쪽으로 끌어당기는 정도를 상대적 수치로 나타낸 것을 의미한다. 파울링 스케일을 기준으로 하였을 때, 티타늄, 지르코늄, 텅스텐, 산소 원자에 대한 전기음성도는 각각 1.33, 1.54, 2.36, 3.44로 대표된다. 물질 A와 B가 가지고 있는 전기 음성도 값 χA과 χB를 Eq. 6에 대입하면, 물질 A와 물질 B 사이의 이온결합 세기를 계산해낼 수 있다. 고에너지 물질의 경우 금속의 산화가 주요한 노화 효과로 대표되기 때문에, 금속 원자(Ti, Zr, W)와 산소 원자가 이루는 이온결합 세기의 정도를 계산하여 각각 비교해보았다.
| (6) |
텅스텐과 산소(W-O)의 경우 ionic character가 약 25%로 계산이 되었으며, 티타늄과 산소(Ti-O) 및 지르코늄과 산소(Zr-O)의 경우, 각각 60%와 67%의 값을 가졌다. 해당 결과는 텅스텐 금속이 티타늄 혹은 지르코늄과 같은 금속과 비교했을 때 산소 원자와 전자를 더 쉽게 공유할 수 있음을 의미한다. 따라서 텅스텐의 경우 노화로 인하여 표면에 산화막이 형성되면 동일한 조건에서 티타늄이나 지르코늄의 경우와 비교해보았을 때 더욱 안정된 특성을 보이게 된다. 이는 다시 말해서 텅스텐 금속 입자가 산화막과 강한 결합을 형성함으로써 텅스텐 금속이 다른 물질과 새롭게 화학반응을 일으키는 것이 어렵게 되고 이에 따라 중간 생성반응이 줄어들게 되는 효과가 나타나는 것이다. 반면에 THPP와 ZPP의 경우 각 금속 원소가 산소와 상대적으로 높은 이온 결합을 형성하기 때문에 텅스텐 금속보다 훨씬 반응성이 좋은 특성을 가지게 된다. 따라서 연소반응을 진행할 때 중간 생성반응이 누락되지 않고, 증가하는 결과가 나타나게 되는 것이다.
5. 결 론
본 연구에서는 연료 역할을 하는 텅스텐 금속과 산화제 역할을 하는 KClO4로 구성된 텅스텐 파이로 지연제 물질에 대하여 DSC와 TGA를 활용하여 열분석을 수행하였으며, 수분 노화를 시켜 해당 시료에서 열역학적 성능의 변화를 확인해볼 수 있었다.
먼저 노화 기간이 늘어남에 따라 DSC에서 측정된 열 유량의 세기 및 발열량이 감소하는 경향이 나타났는데, 10주간 노화시킨 시료를 보면 열 유량의 세기가 약 51%(2.71 W/g→1.31 W/g) 감소하였고, 발열량의 경우도 약 43%(-508 J/g→-290 J/g) 정도 크게 저하되었다. 이러한 열 성능의 감소는 산화제의 사전 분해와 금속 성분의 산화현상으로 인한 조성변화로 인하여 나타난 결과라고 할 수 있다. 텅스텐의 산화로 인하여 나타난 주요한 결과인 잔여 산화제의 분해 현상은 DSC 열분석 결과에 피크 분리 기법을 적용하여 확인해볼 수 있었다.
더 나아가 DSC 실험 결과를 기반으로 프리드만 등 전환법을 적용하여 각 노화 시료에 대한 화학반응인자 또한 추출할 수 있었다. 텅스텐 파이로 지연제의 경우 반응률에 대한 활성화에너지가 총 다섯 가지 스텝으로 구성되어있었다. 바인더의 분해반응, 연료 및 산화제의 연소반응, 잔여 산화제의 분해반응을 나타내는 구간에서 노화 기간이 약 2주로 짧았을 경우에는 활성화에너지가 약간 감소하는 경향을 보이다가 그 이상 노화가 진행되었을 때는 높아지는 경향성을 보였다. 이는 노화 기간 2주를 기점으로 이전에는 산화제의 사전 분해 현상이 우세하게 일어나다가 그 이상 노화 시에는 금속의 산화 현상이 더 강화되는 것을 의미한다고 할 수 있다.
그리고 앞서 수행한 텅스텐 파이로 지연제에 대한 열분석 결과와 고습도 조건에서 노화시킨 THPP 개시제와 ZPP 추진제에 대한 노화 분석 결과를 통합하여 분석을 수행하였다. 이를 통해 수분 노화된 금속-KClO4 산화제 기반의 고에너지 물질의 화학 반응역학의 변화를 이끄는 주요한 요소를 파악해보고자 하였다.
먼저 세 종류의 고에너지 물질 모두 노화가 되었을 때 금속 성분의 산화가 공통으로 나타났으며, 이때 노화 기간에 따라 금속이 산화된 정도가 더 심해지는 경향이 드러났다. 이는 결과적으로 연소반응에 필요한 활성화에너지 평균값의 증가를 가져오게 된다. 따라서 수분 노화된 금속 입자 표면의 산화막 두께가 활성화에너지와 비례 관계를 가지는 것을 파악해볼 수 있다. 한편 금속원소와 산소 간의 전기음성도 차이가 화학반응인자의 표준편차를 좌우하는 요소임을 확인하였다. 예를 들어, 텅스텐의 경우 산소와 약 25%의 이온결합 특성을 보였지만 티타늄과 지르코늄의 경우 산소와 각각 60% 및 67%에 해당하는 높은 이온결합 특성을 보여주었는데, 이는 텅스텐 금속이 산소 원자와 안정한 결합을 형성하여 연소 과정에서 중간 생성반응이 줄어들게 됨을 추정해볼 수 있다. 반면에 티타늄 및 지르코늄은 상대적으로 산소보다는 외부 물질과의 반응성이 더욱 좋기 때문에 중간 생성반응의 증가를 가져오게 된다. 따라서 본 연구에서는 금속 입자와 산소 간의 전기음성도 차이가 연소반응에 있어서 중간 생성반응의 정도를 결정하는 요소로 작용할 수 있음을 처음으로 발견해내었다. 이러한 발견은 고에너지 물질의 성능 설계에 있어서 중요한 참고 데이터로 활용이 가능하며, 추후에는 기대수명 측정에 있어 효과적으로 사용될 수 있을 것으로 기대되는 결과라고 할 수 있다.
Acknowledgments
[이 논문은 한국추진공학회 2022년도 춘계학술대회(2022.5.25.∼27, 라마다프라자 제주호텔) 발표논문을 심사하여 수정ㆍ보완한 것임.]
본 논문은 2022년도 BK21플러스 사업이며, 또한 정부(과학기술정보통신부)의 재원으로 한국연구재단의 지원을 받아 수행된 연구입니다(NRF-2020R1F1A1072007, NRF-2021M1A3B8079020).
References
-
Oh, J., Ambekar, A. and Yoh, J.J., “The hygrothermal aging effects of titanium hydride potassium perchlorate for pyrotechnic combustion,” Thermochimica Acta, Vol. 665, pp. 102-110, 2018.
[https://doi.org/10.1016/j.tca.2018.05.019]

-
Oh, J., Jang, S.G. and Yoh, J.J., “Towards understanding the effects of heat and humidity on ageing of a NASA standard pyrotechnic igniter,” Scientific Reports, Vol. 9, No. 1, pp. 1-12, 2019.
[https://doi.org/10.1038/s41598-019-46608-8]

-
Gnanaprakash, K., Lee, Y. and Yoh, J.J., “Investigation of aging induced processes on thermo-kinetic and combustion characteristics of tungsten pyrotechnic delay composition,” Combustion and Flame, Vol. 228, pp. 114-127, 2021.
[https://doi.org/10.1016/j.combustflame.2021.01.036]

-
Han, B.H., Kim, Y., Jang, S., Yoo, J. and Yoh, J.J., “Thermochemical characterization of Zr/Fe2O3 pyrotechnic mixture under natural aging conditions,” Journal of Applied Physics, Vol. 126, No. 10, pp. 105113, 2019.
[https://doi.org/10.1063/1.5096803]

-
Oh, J. and Yoh, J.J., “Insights into aging mechanism of Ti-metal based pyrotechnics and changes in thermo-kinetic characteristics,” Proceedings of the Combustion Institute, Vol. 38, No. 3, pp. 4441-4449, 2021.
[https://doi.org/10.1016/j.proci.2020.08.040]

-
Naseem, H., Yerra, J., Murthy, H. and Ramakrishna, P.A., “Ageing studies on AP/HTPB based composites solid propellants,” Energetic Materials Frontiers, Vol. 2, No. 2, pp. 111-124, 2021.
[https://doi.org/10.1016/j.enmf.2021.02.001]

-
Kishore, K., Verneker, V.P. and Prasad, G., “Mechanism of ageing of composite solid propellants,” Combustion and Flame, Vol. 36, pp. 79-85, 1979.
[https://doi.org/10.1016/0010-2180(79)90047-6]

-
Tompa, A.S. and William F.B. Jr. “Microcalorimetry and DSC study of the compatibility of energetic materials,” Thermochimica Acta, Vol. 367-368, pp. 433-441, 2001.
[https://doi.org/10.1016/S0040-6031(00)00674-2]

-
Kim, Y., Ambekar, A. and Yoh, J.J., “Toward understanding the aging effect of energetic materials via advanced isoconversional decomposition kinetics,” Journal of Thermal Analysis and Calorimetry, Vol. 133, No. 1, pp. 737-744, 2018.
[https://doi.org/10.1007/s10973-017-6778-2]

-
Sinha, S., Piekiel, N.W., Smith, G.L. and Morris, C.J., “Investigating aging effects for porous silicon energetic materials,” Combustion and Flame, Vol. 181, pp. 164-171, 2017.
[https://doi.org/10.1016/j.combustflame.2017.03.015]

-
Sippel, T.R., Timothée, L.P. and Steven, F.S., “Combustion of nanoaluminum and water propellants: Effect of equivalence ratio and safety/aging characterization,” Propellants, Explosives, Pyrotechnics, Vol. 38, No. 1, pp. 56-66, 2013.
[https://doi.org/10.1002/prep.201200143]

- Nishiwaki, Y., Akiyoshi, M., Matsunaga, T. and Kumasaki, M., “Effect of deterioration products in moisture on the thermal behavior of ammonium perchlorate/magnesium mixture,” Sci. Tech. Energetic Materials, Vol. 79, No. 5, pp. 151-155, 2018.
-
Han, B., Gnanaprakash, K., Park, Y. and Yoh, J.J., “Understanding the effects of hygrothermal aging on thermo-chemical behaviour of Zr-Ni based pyrotechnic delay composition,” Fuel, Vol. 281, pp. 118776, 2020.
[https://doi.org/10.1016/j.fuel.2020.118776]

-
Nie, H.Q., Chan, H.Y., Pisharath, S. and Hng, H.H., “Combustion characteristic and aging behavior of bimetal thermite powders,” Defence Technology, Vol. 17, No. 3, pp. 755-762, 2021.
[https://doi.org/10.1016/j.dt.2020.05.009]

-
Cerri, E. and Barbagallo, S., “The influence of high temperature exposure on aging kinetics of a die cast magnesium alloy,” Materials Letters, Vol. 56, No. 5, pp. 716-720, 2002.
[https://doi.org/10.1016/S0167-577X(02)00601-8]

-
Banhart, J., Chang, C.S.T., Liang, Z., Wanderka, N., Lay, M.D. and Hill, A.J., “Natural aging in Al‐Mg‐Si alloys–a process of unexpected complexity,” Advanced Engineering Materials, Vol. 12, No. 7, pp. 559-571, 2010.
[https://doi.org/10.1002/adem.201000041]

-
Friedman, H.L., “Kinetics of thermal degradation of char‐forming plastics from thermogravimetry. Application to a phenolic plastic,” Journal of Polymer Science Part C: Polymer Symposia, Vol. 6. No. 1., pp. 183-195, 1964.
[https://doi.org/10.1002/polc.5070060121]

-
Vyazovkin, S., Burnham, A.K., Criado, J.M., Pérez-Maqueda, L.A., Popescu, C. and Sbirrazzuoli, N., “ICTAC Kinetics Committee recommendations for performing kinetic computations on thermal analysis data,” Thermochimica Acta, Vol. 520, No. 1-2, pp. 1-19, 2011.
[https://doi.org/10.1016/j.tca.2011.03.034]

- American Institute of Aeronautics and Astronautics (AIAA), Criteria for explosive systems and devices on space and launch vehicles, 1st ed., AIAA, Reston, U.S.A., 2005.
-
Lu, K.T. and Yang, C.C., “Thermal Analysis Studies on the Slow‐Propagation Tungsten Type Delay Composition System,” Propellants, Explosives, Pyrotechnics: An International Journal Dealing with Scientific and Technological Aspects of Energetic Materials, Vol. 33, No. 5, pp. 403-410, 2008.
[https://doi.org/10.1002/prep.200700287]

-
Zhang, Y., Chen, M., Zhang, Z., Jiang, Z., Shangguan, W. and Einaga, H., “Simultaneously catalytic decomposition of formaldehyde and ozone over manganese cerium oxides at room temperature: Promotional effect of relative humidity on the MnCeOx solid solution,” Catalysis Today, Vol. 327, pp. 323-333, 2019.
[https://doi.org/10.1016/j.cattod.2018.04.027]

-
Cheng, Z., Wu, W., Ji, P., Zhou, X., Liu, R. and Cai, J., “Applicability of Fraser–Suzuki function in kinetic analysis of DAEM processes and lignocellulosic biomass pyrolysis processes,” Journal of Thermal Analysis and Calorimetry, Vol. 119, No. 2, pp. 1429-1438, 2015.
[https://doi.org/10.1007/s10973-014-4215-3]