열/수분노화로 인한 Ti 금속 기반의 파이로 물질의 점화 성능 변화와 노화 모델 제시
Copyright Ⓒ The Korean Society of Propulsion Engineers
This is an Open-Access article distributed under the terms of the Creative Commons Attribution Non-Commercial License(http://creativecommons.org/licenses/by-nc/3.0) which permits unrestricted non-commercial use, distribution, and reproduction in any medium, provided the original work is properly cited.
초록
Titanium hydride potassium perchlorate (THPP)는 일반적으로 널리 사용되는 착화제로 추진 시스템에서 중요한 역할을 수행해오고 있지만, ‘노화’라는 현상으로 인하여 THPP의 요구 성능 변화, 심지어는 system failure가 초래될 수 있다. 본 연구에서는 다양한 상대습도 조건에서 노화된 THPP의 열역학적 특성 및 성능, 점화 특성 변화를 상세한 열분석과 점화 실험을 통해 밝혔다. 그리고 형태학적 분석과 조성 변화를 통해 노화에 따른 THPP의 물리⋅화학적인 변화 또한 확인하였다. 결론적으로, 열노화는 산화제 분해로 인하여 활성화 에너지 감소/반응성 증가로 이어지고 수분노화는 연료 산화로 인하여 활성화 에너지 증가/반응성 감소와 같은 경로를 따름을 최종적으로 확인해볼 수 있었다.
Abstract
Titanium hydride potassium perchlorate (THPP) has played an important role as initiators of the propulsion system. However, the ‘aging’ may cause performance degradation and even give rise to a failure in the total system. In this study, various hygrothermal aging conditions were considered and the aging effects on thermodynamic and ignition characteristics of THPP are provided via thermal analysis and ignition measurements. Also, physical-chemical changes were identified by morphological analysis. In conclusion, thermal aging led to Eα decrease-high reactivity due to oxidizer decomposition whereas hygrothermal aging gave rise to an opposite tendency by fuel oxidation.
Keywords:
Titanium Hydride Potassium Perchlorate, Ignition Characteristics, Pyrotechnics, Aging Analysis키워드:
THPP, 점화 특성, 파이로물질, 노화 분석1. 서 론
Titanium hydride potassium perchlorate (THPP)는 로켓이나 미사일과 같은 발사⋅추진 시스템에서 전기적 입력을 인가받아 압력을 생성해내는 일반적으로 사용되는 파이로 착화제 중 하나이다. 1960년대부터 사용되어온 THPP는 자동차의 에어백에서부터 우주 추진 시스템에서까지 크고 작은 분야에서 널리 활용되는 중요한 물질이라고 할 수 있다. 이렇게 파이로테크닉 착화제는 전체 시스템의 개시를 담당하는 결정적인 역할을 수행하기 때문에 필요한 순간에 정확한 성능 발현이 요구된다. 그런데 시간이 지남에 따라 파이로테크닉 착화제 내부의 물질들이 서로 상호작용을 일으키고 이에 따라 조성 비율의 변화를 초래할 수 있다. 이러한 변화는 결국에 생성 압력에 영향을 미치게 되어 설계 성능에 도달하지 못하게 되는 결과를 가져올 수 있을 뿐만 아니라 최악의 경우 개시 실패로 이어질 수 있어 시간⋅비용⋅안전적인 측면에서 악영향을 끼칠 수 있다. 따라서 ‘노화’라는 파라미터는 추진시스템 설계에 있어서 필수적으로 고려해야 하며 최근 들어 고에너지물질에 있어서 노화의 중요성에 대해 큰 주목을 받고 있다.
이렇게 노화의 중요성이 대두됨에 따라, 고에너지 물질에 대한 실험 및 연구가 활발히 진행되고 있다. 노화 연구 관련해서는 주로 열분석을 통한 연소속도, 발열량, 점화지연시간, 반응성의 변화를 통해 반응 메커니즘을 구축하였으며[1-9], 분광학적 계측[6,9-11], 형태학적 분석 및 X선 분산[1-6] 결과를 통한 해석과 더불어 연소 실험[11,12] 기반 결과를 활용하여 노화의 영향과 효과 분석에 대한 연구가 활발하게 진행되어오고 있다.
THPP 착화제와 관련해서도 열량 분석을 통하여 새로운 노화 현상들이 발견된 바 있다[2,7,8]. 먼저 THPP를 이루고 있는 구성 물질 각각에 대한 열분석을 수행한 후, 각 물질이 THPP mixture에 미치는 노화 효과를 확인하여 노화에 취약한 성분을 파악하는 연구가 수행된 바 있다[7,8]. 그런데 대기 중에는 산소뿐만 아니라 상당량의 수증기도 포함되어 있기 때문에, 노화 파라미터로 상대습도 또한 고려되어야 정확한 성능 감소를 파악할 수 있을 것이다. 그런데 이전 연구 동향들을 분석해보면, THPP 착화제에 대한 수분노화 관련 연구는 미흡한 편이다. 이전 연구에서 수분노화가 THPP의 성분 및 성능에 미치는 영향을 확인한 바 있지만[2], 제한된 노화 기간과 상대습도 함량이 0%와 100% 조건에서만 비교를 진행하였기 때문에 중간 범위의 습도 레벨에서의 정확한 노화 효과 규명은 어렵다고 할 수 있다.
따라서 본 연구에서는 보다 다양한 습도 조건(0%, 30%, 70%)과 노화 기간을 고려하여 THPP 착화제에 대한 수분노화효과를 열분석을 통해 보다 상세하게 규명하고자 하였다. 그뿐만 아니라 field emission scanning electron microscopy-energy dispersive spectroscopy(FE-SEM-EDS)를 통하여 형태학적/화학적 변화 또한 관찰할 수 있었다. 그리고 thermo-gravimetric analysis(TGA)를 통해 얻은 결과를 바탕으로 Friedman isoconversional method를 적용함으로써 반응 진행에 따른 화학반응인자들을 획득하였다. 또한 점화 실험도 수행함으로써 연소 지연시간과 발화 온도와 같은 중요한 점화 특성 또한 확인할 수 있었다. 따라서 노화에 따른 점화 특성과 연소 특성 변화에 대한 새로운 연관관계를 파악할 수 있었고, 실험을 통해 획득한 데이터를 바탕으로 THPP 성능에 있어서 온도 및 상대습도가 끼치는 영향을 반영하여 노화 메커니즘을 구축할 수 있었다.
2. 실 험
2.1 실험 재료
본 연구에서 사용된 THPP는 30%의 TiH2 (Rookwood Lithium Ltd.), 65%의 KClO4 (Barium & Chemical Inc.), 5%의 Viton-b (Dupont Ltd.)로 구성되어 있다. 해당 THPP 물질에 대하여 Table 1과 같이 각 조건에 따라 노화된 시료를 사용하였다.
2.2 상세 노화 조건
본 연구에서는 열노화와 수분노화된 시료를 사용하여 열분석을 수행하였으며, 특히 수분노화의 경우 30%와 70% 조건으로 상대습도 조건을 달리하여 습도 레벨에 따른 THPP 성능 변화를 확인하고자 하였다. 이때, 노화 조건에서 G0은 비노화 시료, G1은 열노화 시료(0% RH 조건), G2는 30% RH 조건에서 수분노화 된 시료, G3은 70% RH 조건에서 수분노화 된 시료를 의미한다.
노화 공정은 THPP 시료를 71 ℃의 온도로 유지되고 있는 열풍 순환식 오븐 내에 4.7 L의 용기에 시료를 밀폐시킨 상태에서 저장시켜 노화를 가해주었다. 각 습도 조건은 4.7 L의 용기 부피에서 상대습도 조건에 맞는 정제수의 양을 투입하여 조절할 수 있었다. 이때, 정제수의 양은 온도 71 ℃ 조건에서의 수증기압과 이상기체 상태방정식을 적용하여 계산되었다.
시료의 입도는 200 mesh sieve에 걸러 75 μm 이하로 구성되도록 하여 입자 크기에 따른 열분석 결과의 차이를 최소화 하고자 하였다. 비록 본 연구에서 설정한 입도는 electric-explosive initiator의 표준 규격[13]은 아니지만 THPP 제조 시 Viton 혼합 공정에서 발생하는 응집현상과 SEM image 결과를 반영해보면 75 μm 입자 크기가 적절할 것이라고 판단하였다.
2.3 FE-SEM-EDS 분석
In-lens Schottky plus 전계 방출 전자총과 EDS와 결합된 2 차 검출기가 장착된 전계 방출 주사 전자 현미경(JSM-7800F Prime, JEOL Ltd, Japan)을 사용하여 노화되지 않은 THPP 샘플의 SEM 이미지를 캡처하여 각 물질의 형상과 농도를 파악하였다. SEM 분해능은 1.00 nm(15 kV) 및 2.2 nm(1 kV)이며 SEM-EDS는 샘플 표면의 형태 정보와 원소 조성을 제공한다.
2.4 열분석(DSC & TGA)
연소과정이 이루어지는 동안 THPP는 급격한 열 방출과 물리적 및 화학적 변화를 수반하며, 이 과정에서 중요한 연소 특성들을 얻을 수 있다. 이때, 노화로 인한 고에너지 물질의 연소 및 열 특성 변화는 노화 분석에 있어서 필수적인 정보를 제공한다. 본 연구에서는 DSC와 TGA를 사용하여 열분석 실험을 진행하였으며, International Confederation for Thermal Analysis and Calorimetry Kinetics Committee’s recommendations[14]를 따름으로써 보다 정확한 결과를 얻고자 하였다. 열분석 수행 시 사용한 장비는 Mettler Toledo 사의 DSC-3+와 TGA 2이다. 각 파우더 시료는 DSC의 경우 standard 40 μL aluminium crucible(0.5 mm perforated closed pan)에 TGA의 경우 70 μL alumina crucible(open pan)에 약 2∼3 mg가량 사용되었다. 이때, 시료는 열이 집중되거나 편향되는 효과를 막기 위해 팬에 최대한 평평하게 담아 실험을 진행하였다. 수행 온도 범위는 30 ℃∼600 ℃이며, 승온 속도를 1, 2, 4, 8 ℃/min로 다르게 하여 실험을 수행하였으며, 이때 열이 고여 있는 현상을 막기 위해서 80 ml/min의 질소 퍼지가스가 흐르는 상태에서 실험이 진행되었다.
2.5 Reaction kinetics 계산
본 연구에서는 가장 널리 사용되는 방법 중 하나인 Friedman isoconversional method를 적용하여 해당 시료들에 대한 화학반응 인자들을 계산해내었다[14,15]. 이때, 사용된 실험 데이터는 non-isothermal condition 조건으로 수행된 TG 실험 기반이다. Differential isoconversional method 방법 중 하나인 Friedman isoconversional method는 DSC와 같은 미분 기반 실험 데이터와 같이 사용하면 보다 상세한 데이터를 얻을 수 있지만 노이즈가 심한 단점이 있어 본 연구에서는 적분 기반 실험데이터인 TGA 실험 데이터를 사용하여 발생하는 노이즈를 최대한 줄일 뿐만 아니라 연소 시 발생하는 산화&분해 현상에 집중하고자 하였다.
Friedman isoconversional method는 아래 Eq. (1)과 같이 Arrhenius equation 기반으로 계산이 수행되며, 이때 Eq. (1)과 Eq. (3)은 등온 조건일 때, Eq. (2)와 Eq. (4)는 비등온 조건인 경우를 의미한다. 본 연구에서는 다양한 승온 속도 β (℃/min)를 활용하여 반응 인자 α에 따른 활성화 에너지와 지수 앞 인자, 즉 빈도 인자를 구할 수 있었다.
| (1) |
| (2) |
| (3) |
| (4) |
이때, 식에서 E와 A는 활성화 에너지(kJ/mol)와 빈도 인자(1/s)를 의미한다. 그 외 α, t, R, T, f(α)는 반응 인자, 시간(s), 이상기체상수(kJ/K⋅mol), 온도(K), 반응 모델로써 정의된다. 그리고 아래 첨자 α로 되어있는 파라미터는 각 반응 인자에 대한 파라미터 값을 의미한다.
2.6 점화 특성 계측 실험
본 연구에서는 ignition delay time(IDT), 점화 온도와 같은 중요 점화 특성 파라미터에 대한 실험을 진행하여, 노화가 해당 특성에 끼치는 영향을 파악하고자 하였다. 이때, IDT는 시료에 전기적 입력을 인가한 순간부터 시료가 최초로 발화하기까지 걸린 시간을 의미한다[6]. Fig. 1에서 점화 실험에 대한 보다 자세한 셋업을 제시해주고 있는데, Fig. 1(a), (b)와 같이 스테인리스 판위에 약 2-3 mg 가량의 THPP 파우더 시료를 올려놓고 직경이 0.3 mm, 길이가 70 mm인 니크롬선을 통해 THPP 시료에 에너지를 인가하였다. 이때, Fig. 1(c)처럼 열선과 판이 맞닿게 되면 열선을 통해 공급되는 열에너지가 판으로 직접적으로 열 손실이 크게 발생하기 때문에 Fig. 1(d)와 같이 열선과 판 사이의 접촉을 피함으로써 열손실을 최소화하였다. 그리고 외부 트리거 시스템과 초고속 카메라(Phantom V711, resolution of 800 pixel x 600 pixel, 105 mm NIKKOR micro-lens)와 전원 공급장치를 연결하여 트리거 시스템을 통해 니크롬선에 전류를 흐르게 하고 동시에 초고속 카메라 촬영을 가능케 하였다.
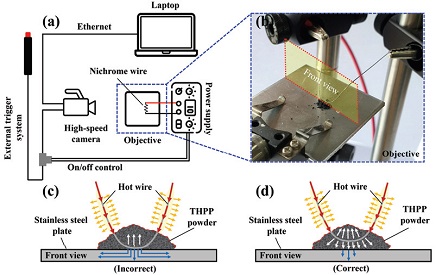
Schematic view of the ignition experimental setup. (a) An experimental setup, (b) enlarged view of an objective, (c) potential heat transfer effects when wire in contact with the plate, and (d) when wire not in touching the plate.
이때, 전원 공급장치 설정은 고정 전압 30 V 하에 전류를 3.0 A에서 4.5 A까지 0.25 A 간격으로 증가시켜가며 에너지 크기에 따른 IDT 변화를 측정하였다[16]. 이때, 점화 온도의 경우 열전대를 통해 측정하여 얻는 것이 가장 정확하나, 본 연구에서는 순간적인 전류 및 전압 조건에서 니크롬선 저항 특성을 통해 계산되는 온도로 예상 점화 온도를 계산하였다.
즉, 줄열을 통해서 가열된 니크롬선의 온도를 통해 점화 온도를 예측하였는데, 니크롬선의 오차를 ±0.5 mm라고 가정하였을 때 측정 및 계산 과정에서 예상되는 오차는 최소 1 ℃에서 최대 10 ℃로 추정된다. 실험 결과의 신뢰성을 높이기 위하여 각 전류 값에 대하여 3회 이상의 점화 실험을 반복하여 진행하였다.
3. 실험 결과
3.1 FE-SEM-EDS 분석 결과
Fig. 2와 같이 SEM-EDS 분석을 통하여 각 시료 구성에 대한 형태와 농도들을 비교해보았다.
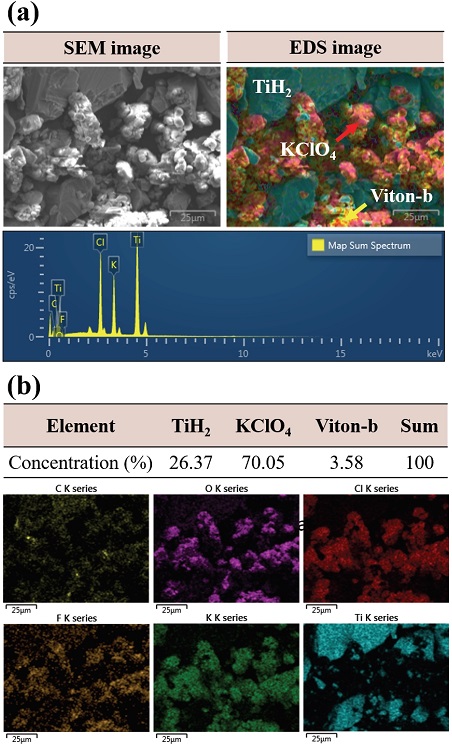
(a) SEM-EDS results of the unaged THPP, (b) obtained composition ratio and profiles of THPP from EDS results.
TiH2는 각진 형태의 평평한 모양을 가진 반면 KClO4 입자는 둥글한 형태를 띠었다. Viton-b는 주로 산화제 입자 겉에서 발견되었다. Fig. 2(b)의 EDS 결과와 같이 각 시료를 구성하는 원소 성분 O, F, K, Cl, Ti, C에 대한 농도 확인이 가능하였으며, 조성을 계산해본 결과 약간의 오차는 있었지만 상당히 유사한 비율을 가졌다.
한편, Fig. 3에서는 노화된 THPP 시료에 대한 SEM-EDS 결과 분석이 가능하다. Fig. 3(a)의 경우 비노화 시료(G0)에 대한 SEM 이미지와 이미지 상에서 나타난 각 원소 O, F, Ti에 대한 농도를 보여주고 있다. 열노화된 THPP(Fig. 3(b))의 경우 Viton-b에 해당하는 F 신호의 농도가 약해져 Viton의 열화가 나타난 것을 볼 수 있다. 반면, 수분노화된 시료의 경우(Fig. 3(c-d)), Ti에 해당하는 부분에 상당한 O의 신호가 발견됨에 따라 상당한 금속 연료의 산화가 진행되었음을 알 수 있다.

SEM-EDS results of the utilized THPP samples. (a) Unaged(G0), (b) thermally aged(G1), (c) 30% RH(G2), and (d) 70% RH(G3).
그런데 SEM 촬영 결과 노화된 THPP 시료에서 특이한 점을 발견하였다. Fig. 4와 같이 노화된 시료에서 산화제 입자에 상당한 crack이 발생하였음을 확인해볼 수 있었다. Fig. 4(a)는 비노화 시료, (b)는 열노화 시료, (c)는 30% RH 조건에서 수분노화된 시료, (d)는 70% RH 조건에서 수분노화된 시료를 의미하는데, 노화된 시료들에서 상당히 긴 길이의 crack들이 형성된 것으로 보아, 노화 현상으로 인하여 산화제 분해가 진행되었음을 추정해볼 수 있으며 비슷한 연구가 진행된 관련 연구 또한 발견되었다[17]. 이는 이전에 수행하였던 THPP 수분노화 연구[2] 결과와 일치하는 결과이며, 따라서 노화가 THPP의 산화제 분해를 촉진하는 역할을 가져올 수 있다는 것을 형태학적으로 증명한다고 할 수 있다.
3.2 DSC 열분석 결과
THPP에 대하여 DSC 실험을 수행해본 결과 30 ℃와 600 ℃ 사이에서 두 종류의 발열반응이 나타나는 것을 확인해볼 수 있었다. 따라서 본 연구에서는 각 발열반응에 대한 상세한 분석을 수행하기 위해 two-step으로 나누어 해석을 진행하였다.
Fig. 5의 경우 THPP의 primary thermal reaction에 대한 결과를 나타내며, Fig. 5의 경우는 THPP의 secondary thermal reaction을 보여주고 있다.
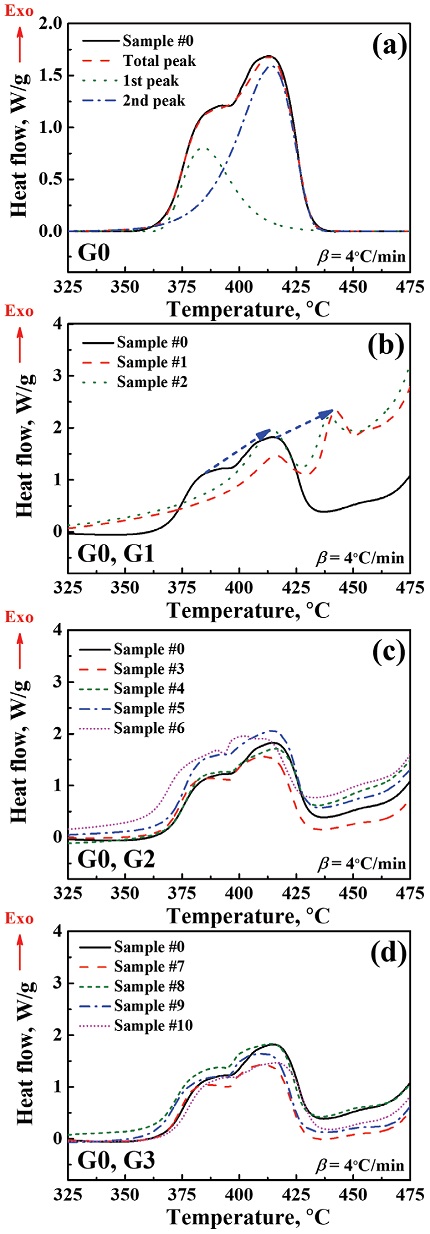
(a) Primary reaction of THPP, (b) thermal aging effects, (c) aging effects on G2, and (d) aging effects on G3.
Fig. 5(a)에서 THPP의 primary reaction에 대하여 피크 분리 기법을 수행하여 전체 발열반응을 구성하고 있는 세부 반응들을 확인하였다. Primary reaction의 경우, 두 종류의 발열반응으로 구성이 되어있음을 확인해볼 수 있었다. 첫 번째 발열반응은 Viton-b의 분해반응[8,18]으로 정의될 수 있으며 두 번째 발열반응은 THPP의 pre-combustion 반응[18]으로 추정된다. Fig. 5(b)-(d)는 노화군에 따라 primary reaction의 변화가 어떻게 발생하는지 보여주고 있는데, 열노화의 경우 두 종류의 발열반응 온도가 상당히 지연되었으며 각각의 발열반응이 뚜렷하게 구분되어 있었다. 이는 THPP가 오랫동안 열에 노출이 되었을 때, 바인더의 열화와 더불어 산화제 성능 감소도 초래될 수 있음을 보여주고 있다. 수분노화 시킨 시료의 노화 기간은 열노화된 시료의 노화 기간보다는 짧은 관계로 노화 기간에 따른 열 반응의 큰 변화는 발생하지 않았다. 하지만 노화 기간이 증가함에 따라 기준선의 기울기가 변형이 되고, 예연소에 해당하는 반응이 감소하는 결과를 보여 수분노화의 경우 바인더보다는 산화제에 더 영향을 끼친다는 것을 알 수 있다.
뿐만 아니라 30% 상대습도 조건에서 노화된 시료는 기준선이 상향되는 경향을 보였으며, 70% 상대습도 조건에서 노화된 시료는 기준선이 하향되는 경향을 보여주었다. 전반적으로 낮은 상대습도 조건에서 기준선의 기울기는 비노화 시료 기준으로 높은 값을 가지며, 높은 상대습도 조건의 경우 작은 값을 가지는 것이 확인되었다. 이에 따라 상대습도 조건이 시료의 기준선의 기울기에도 영향을 끼칠 수 있음을 보여주고 있다.
Secondary thermal reaction을 나타내는 Fig. 6의 경우, 피크 분리 기법을 적용해본 결과(Fig. 6(a)) 두 번째 발열반응은 첫 번째 발열반응 보다 상당히 복잡한 반응으로 구성되어 있음을 확인해볼 수 있었다. 두 번째 발열반응은 총 5가지의 세부 반응들로 구성이 되어있었는데, 해당 반응은 다음과 같이 나타낼 수 있다.
- 1. KClO4 decomposition[18]
- 2. TiH2 dehydrogenation[19]
- 3. Formation of water vapor[20]
- 4. Combustion of THPP[2]
- 5. Decomposition of remaining KClO4[18]
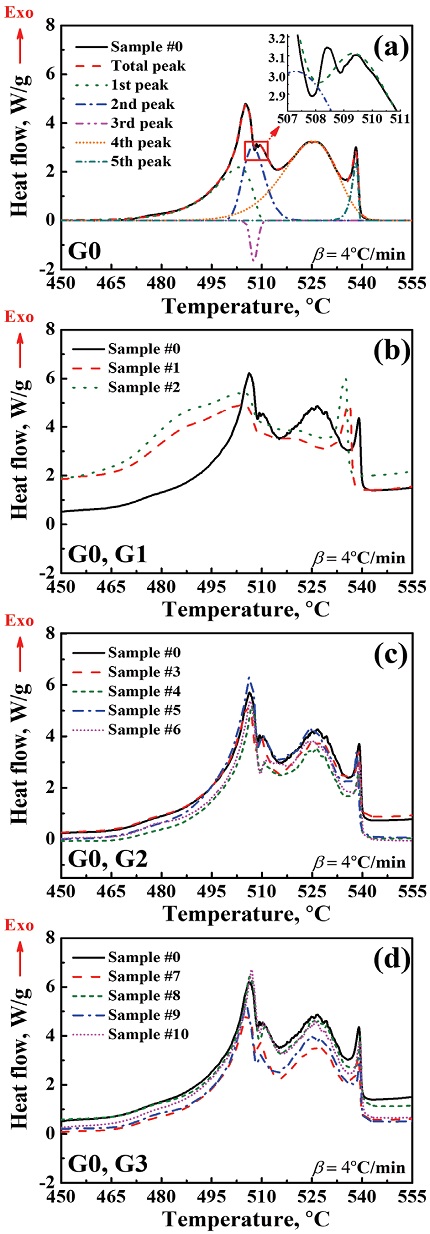
(a) Secondary reaction of THPP, (b) thermal aging effects, (c) aging effects on G2, and (d) aging effects on G3.
이때, 흡열반응인 TiH2 분해 현상의 경우 DSC 실험에서 약 508 ℃와 509 ℃ 부근에서 나타났는데, 실험과 이론적인 발생 온도 값(509∼535 ℃)[19] 이 상당히 잘 일치하였음을 알 수 있다. 노화된 시료에 대한 결과는 Fig. 6(b)-(d)에서 확인해볼 수 있는데, 열노화된 시료의 경우 산화제 분해 현상이 낮은 온도에서 시작하여 급격하게 발생한 반면에 THPP 연소과정은 약화되었다. 이는 앞서 SEM 이미지 결과에서도 확인했듯이 KClO4 산화제가 분해가 되어 나타난 결과라고 할 수 있다. 반응성이 더 좋은 KClO3로 인하여 낮은 온도에서부터 산화제 분해가 시작되었고, 먼저 분해된 산화제로 인하여 THPP 연소과정에서 충분한 산소를 공급받지 못하였기 때문에 THPP 연소 성능이 떨어졌다고 추정해볼 수 있다. 수분노화의 경우, 첫 번째 발열반응과 같이 큰 변화는 없었지만 기준선의 기울기를 비롯하여 수증기 생성 반응에서 변화를 보였고, 전체적으로 열유량의 크기가 감소하는 경향을 가졌다. 따라서 해당 결과로부터, 수분 조건에 THPP 연소 성능에 있어서 불안정성을 야기할 수 있으며 열 성능 감소로도 이루어질 수 있음을 나타낸다.
3.3 발열량 성능 변화
수행한 DSC 실험 결과를 바탕으로 발열량을 측정해본 결과 Table 2와 같이 나타낼 수 있다. 해당 발열량은 1, 2, 4, 8 ℃/min에서 측정된 발열량을 평균한 값이며 발열량 오차가 10% 미만이다. 일반적으로 THPP와 유사한 TiH1.65/KClO4 물질의 경우, 발열량이 6500 J/g이라고 알려져 있다[21]. 그런데 본 연구에서 실험을 통해 얻어진 발열량의 경우 6500 J/g보다는 낮은 값을 가졌는데, 그 이유로는 TiHx 성분에서 수소 성분 함량의 차이와 본 시료에서는 Viton이 포함되어있고 TiO2 성분 또한 미량 함유되어 있기 때문에 낮은 발열량을 보였다고 추정해볼 수 있다. 그리고 실험이 수행되는 동안 팬 내부에서 발생한 열 손실도 고려해야 할 것이다. 발열량 측정 결과 열노화 시료의 경우 첫 번째 발열반응에서 발열량이 30∼40%가량 상당히 감소한 것을 확인해볼 수 있었다.
반면 수분노화된 시료는 두 번째 발열반응에서 30% 상대습도 조건에서는 최대 35%, 70% 상대습도 조건에서는 최대 40%의 발열량 감소를 가졌다. 그리고 공통적으로 노화 기간이 늘어남에 따라 발열량이 비례해서 감소하는 경향을 보였으며, 상대습도가 증가할수록 발열량 감소 폭은 최대 40%까지 증가하였다.
그래서 해당 결과로부터 열노화의 경우 Viton 열화 및 산화제 분해 현상을 초래하여 첫 번째 발열반응의 열 성능을 크게 감소시킬 수 있으며, 수분노화의 경우 주요 연소 반응에 해당하는 발열량 감소를 초래할 수 있음을 시사한다.
3.4 TGA 열분석 결과
모든 THPP 시료에 대하여 2 ℃/min 승온 조건에서 30∼640 ℃까지 TGA 실험을 수행해본 결과 Fig. 7과 같이 나타낼 수 있다. Fig. 7(a)는 전체 온도 범위에 대한 결과를 보여주고 있다. Fig. 7(b)는 primary thermal reaction에 해당하는 온도 범위를, Fig. 7(c)는 secondary thermal reaction에 해당하는 온도 범위를 따로 확대하였다. TGA 결과는 앞서 DSC 실험 결과에서 확인한 바와 같이 각 반응 온도 범위에서 무게가 감소하는 two-step reaction을 보였으며, primary reaction에서 Viton-b의 구성비에 해당되는 5%만큼 질량 감소를 보여 해당 반응이 Viton의 분해반응이라는 것을 검증해볼 수 있었다[8].
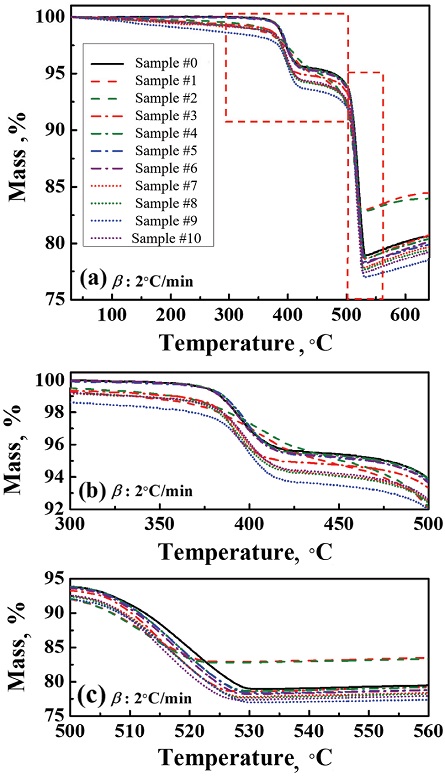
(a) TGA results of THPP samples, (b) enlarged view of the first step, and (c) enlarged view of the second step.
이때, 노화된 시료의 경우 노화 조건마다 다른 경향성들을 확인해볼 수 있었는데 열노화의 경우 primary reaction에서 secondary reaction으로 가는 도중에 induction period가 없이 지속적으로 무게가 감소하는 경향성을 보였다. 해당 반응은 열노화 시 발생한 Viton의 열화 현상으로 인해 발생한 것으로 추정된다. 그뿐만 아니라 secondary thermal reaction 완료 후 잔여 물질의 무게가 다른 시료들에 비해 잔여물 함량이 많은 것을 볼 수 있었다. 수분노화 시료의 경우 일반적인 two-step reaction으로 진행되었지만 수분함량이 증가할수록, 노화 기간이 증가할수록 잔여 물질 무게가 줄어드는 경향성이 나타났다.
이는 열노화 시, 노화 과정에서 시료에 흡착되어 있던 수분이 빠져나가기 때문에 TGA 실험 시 다른 시료들과 비교했을 때 잔여 무게가 높음을 알 수 있다. 반면 수분노화 시료의 경우, 열노화된 시료와는 반대로 노화 과정에서 시료 표면에 수분이 흡착이 되고, 이로 인하여 TGA 실험 시 수분이 증발하면서 상당량의 무게가 줄어들게 되는 것이다.
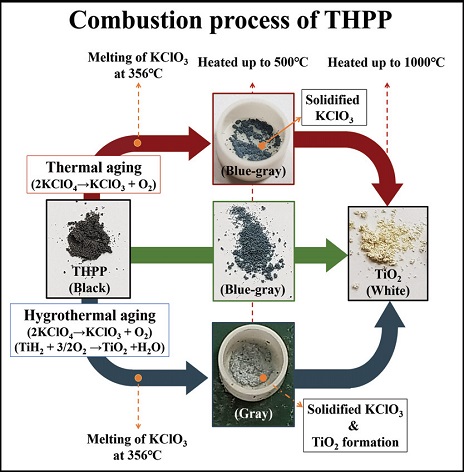
따라서 본 연구에서 수행한 DSC와 TGA 열분석 실험 결과를 토대로 Fig. 8과 같이 THPP 연소과정에 따른 노화 효과를 확인해볼 수 있다. 일반 비노화 THPP 시료를 상온에서 1,000 ℃까지 가열시켰을 때, 500 ℃ 부근에서 blue-gray 색상의 고형 시료로 변하게 된다. 이는 일부 TiH2(검은색)가 산소와 반응하여 TiO2(흰색)로 변하여 나타나는 색상 변화라고 할 수 있다. 1,000 ℃까지 반응이 진행이 되면 시료 전체가 반응에 참여하게 되고, 이에 따라 TiH2연료도 TiO2로 변하게 되어 전부 흰색의 시료로 보이게 된다.
이때, 열 및 수분노화시킨 시료의 경우 산화제 분해로 인하여 KClO3가 생성되기 때문에 약 356 ℃에서 KClO3의 액화가 발생하게 되고, Fig. 8에서와 같이 액체 상태로 되었다가 다시 굳어진 시료의 모습을 확인해볼 수 있었다. 그런데 수분노화의 경우, 노화 과정에서 시료에 흡착된 수분으로 인하여 연료의 산화가 가속되며, 이미 시료 내부에서도 상당량의 산화 금속이 존재하고 있기 때문에 Fig. 8에서 500 ℃에서 회색빛으로 바뀐 시료의 색깔을 나타내게 된다.
3.5 화학반응 인자 분석
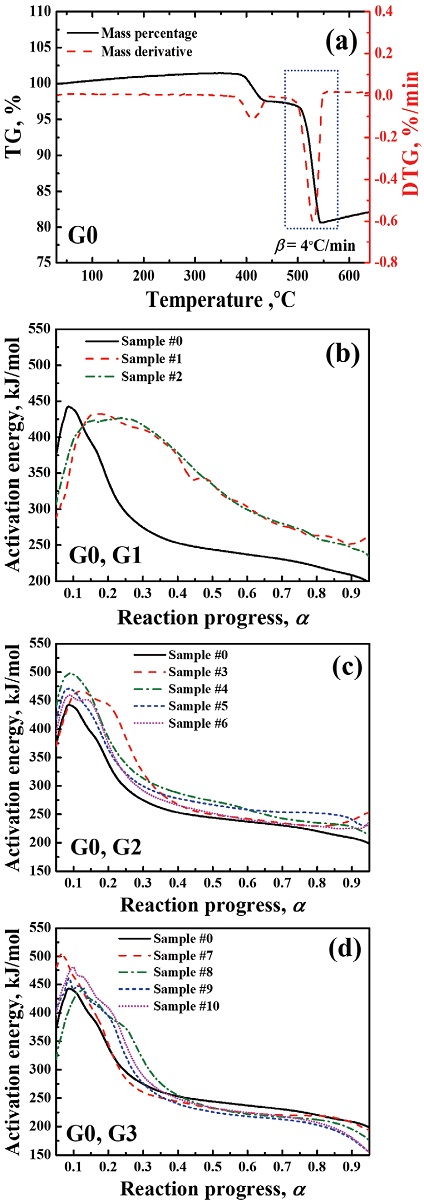
THPP 시료에 대하여 수행된 TGA 실험 데이터를 기반으로 Friedman isoconversional method를 적용하여 반응 인자(α)에 대한 화학반응 인자들을 계산하여 노화의 영향을 확인해 보았다. 본 연구에서는 가장 대표적인 화학반응 인자라고 할 수 있는 활성화 에너지 값에 대하여 primary reaction과 secondary reaction에 따른 변화를 제시하였다. Fig. 9의 경우 primary thermal reaction에 대한 활성화 에너지의 변화를 나타낸다. 상대습도 조건에 따라 시료의 활성화 에너지는 상반된 결과를 보였다.
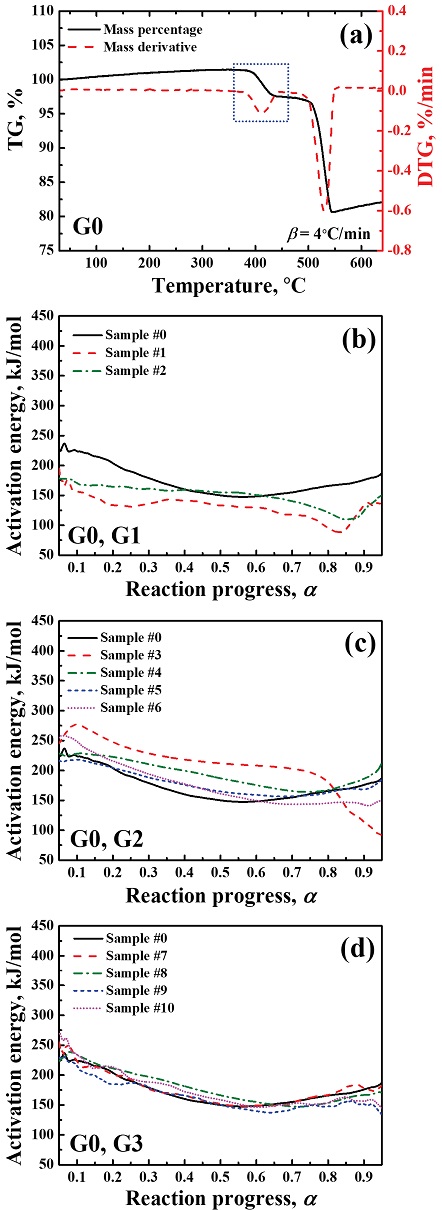
Activation energy for the primary reaction. (a) TG and DTG results of THPP and aging effects on (b) G1, (c) G2, and (d) G3.
열노화의 경우(Fig. 9(b)) 약 80∼170 kJ/mol의 활성화에너지 값을 가져, 150∼230 kJ/mol의 비노화 시료보다 작은 값을 가진 반면에 수분노화의 경우(Fig. 9(c,d)) 최대 270∼280 kJ/mol까지 증가한 활성화 에너지 값을 가졌다. 이는 열노화에서는 산화제 분해 작용이 주된 반응으로 수행 되며, 수분노화에서는 연료 산화 반응이 더 우세하기 때문에 나타난 결과라고 해석해볼 수 있다. KClO3의 경우 KClO4보다 반응성이 더 우수하기 때문에 더 적은 에너지가 공급되어도 쉽게 반응하며, TiO2의 경우 에너지 준위가 높은 안정성이 큰 물질이기 때문에 더 많은 에너지를 공급해 주어도 반응하기가 쉽지 않다.
Fig. 10에서 나타난 secondary reaction에 대한 활성화 에너지의 변화에서는 열노화된 시료는 반응률이 약 20% 정도 우측으로 이동하는 현상을 보였고, 수분노화된 시료는 활성화 에너지 값이 약 10∼15% 정도 상향하는 결과를 보였다. 이는 열노화 시료에서 포함된 KClO3가 secondary reaction 초반에 활성화 에너지를 낮춰주는 역할을 하지만 수분노화 시료의 경우 산화제 분해 현상에 비해 산화 현상이 더 우세하기 때문에 기존 시료보다 더 에너지 장벽이 높아진 것을 볼 수 있다.
3.6 연소 지연시간 측정 결과 분석
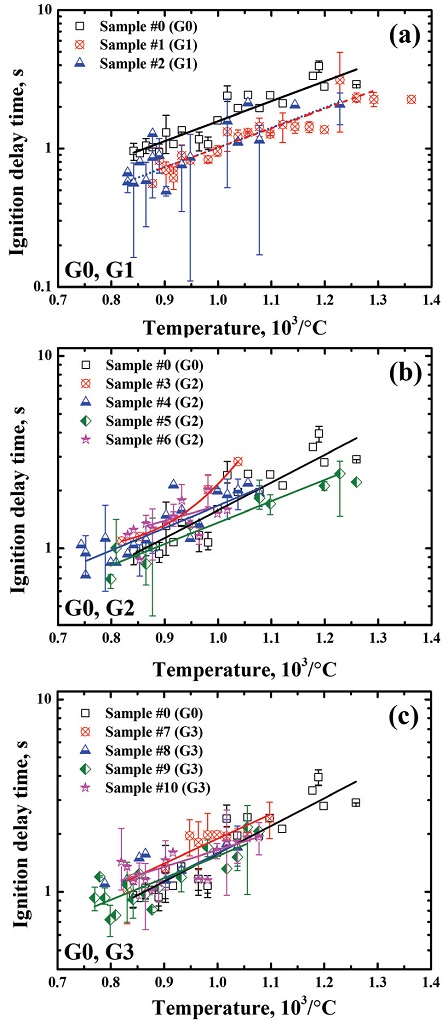
모든 THPP 시료들에 대하여 점화 실험을 진행하였으며, 각 노화군에 대하여 IDT를 측정해본 결과 Fig. 11과 같이 나타낼 수 있었다.
이때, Fig. 11(a)에서는 열노화시킨 시료에서 발견된 노화 효과를 확인해볼 수 있는데, 노화가 진행됨에 따라 약 0.3 s 가량 IDT가 줄어드는 현상을 볼 수 있었다. 즉, 점화 온도에 따른 IDT의 경향성은 비노화 시료와 상당히 유사하지만 y축 방향으로 아래로 이동한 것이다. 이때, 노화 기간이 길어질수록 오차의 범위는 증가하였다. 따라서 열노화가 IDT의 감소를 초래하지만, 노화 기간이 길어짐에 따라 연소 안정성이 약화되는 현상 또한 확인해볼 수 있었다. IDT 감소의 원인으로는 앞선 실험 결과에서도 확인해볼 수 있었듯이 산화제 분해 현상으로 인한 KClO3 생성 및 연소반응을 들 수 있다.
수분노화 시킨 시료의 경우에는 열노화 시료와 사뭇 다른 경향성을 나타냈다. 노화 시 수분이 함유되어 있으면, 점화 온도에 따른 IDT의 기울기가 더욱 완만해지며 IDT 값 자체도 최소 0.1 s에서 최대 1 s까지 지연되는 경향을 보였다. 그뿐만 아니라 점화 온도가 약 900 ℃ 이하에서는 점화 반응이 발생하지 않는 경우가 발생하였다. 이는 상대습도 레벨이 증가할수록 더욱더 뚜렷하게 나타났다. 따라서 노화 조건에서 수분이 TiO2의 함량을 증가시키게 되고, 이는 다시 연소반응의 둔감화로 이어지게 된다. 따라서 IDT가 증가하게 되고 점화 온도도 높아지게 되는 결과가 나타나게 됨을 추정해볼 수 있다.
3.7 THPP의 노화에 따른 연소 및 점화 특성 결과
각 시료들에 대하여 전기적 에너지를 인가하여 점화 실험을 진행하였으며, 초고속 카메라로 촬영한 이미지들이 Fig. 12에 나타나있다. Fig. 12에서 (a)는 비노화 THPP, (b)는 열노화된 시료, (c)는 30% RH 조건에서, (d)는 70% RH 조건에서 노화된 시료를 의미하며, 위에서 아래로 갈수록 시간이 진행되고 있는 상태이다. 이때, IDT는 시료에 전기적 입력을 인가한 순간부터 시료가 최초로 발화하기까지 걸린 시간을 의미한다.
실험 결과를 확인해보면, 비노화 시료와 각종 노화 시료 간의 연소반응에 있어서 상당한 차이를 확인해볼 수 있었다. 먼저 비노화 시료의 경우(Fig. 12(a)), 파트 3.2에서 확인한 바와 같이 THPP의 연소반응이 진행되면서 수증기 발생 현상을 확인해볼 수 있었다. THPP 입자에서 수증기가 방출되고 나서 입자가 개별적으로 터지면서 연소반응이 진행되는 현상을 보였다.
반면 열노화된 시료의 경우, 시료가 빛이 방출되면서 서서히 소멸되는 양상과 함께 매우 짧은 연소시간을 가졌다. 또한, 방출되는 수증기의 양 또한 적었는데, 이는 노화과정에서 H2O 흡착 과정이 상대적으로 적게 발생하고 TiH2 입자 겉을 둘러싸고 있는 얇은 산화막 때문이라고 할 수 있다[22]. 수분노화된 시료의 경우 연소과정에서 상당한 양의 수증기가 방출되고, 연소 반응이 간헐적으로 진행되는 모습을 확인해볼 수 있었다. 이는 시료 표면에 흡착된 수증기가 많아, 상대적으로 두꺼운 산화막이 TiH2에서 수소가 분리될 때 산소를 공급하게 되어 과량의 수증기가 발생했다고 추정해볼 수 있다[22].
그리고 각 노화군에 대하여 연소 시간을 평균을 내본 결과, G0는 0.148 s, G1은 0.023 s, G2는 0.249 s, G3는 0.428 s로 측정되었다. 열노화 시료는 약 0.16배 정도 연소시간이 감소하였으며, 수분노화 시료는 G2와 G3가 각각 1.68배, 2.89배 늘어난 수치를 가졌다. 연소시간도 연소 지연시간과 동일한 경향성을 보였으며, 전반적으로 열노화로 인하여 분해된 생성물인 KClO3가 반응성을 높이고 수분노화로 인하여 생성된 TiO2가 THPP의 반응성을 둔감 시키는 것으로 점화 실험을 통해 확인해볼 수 있었다.
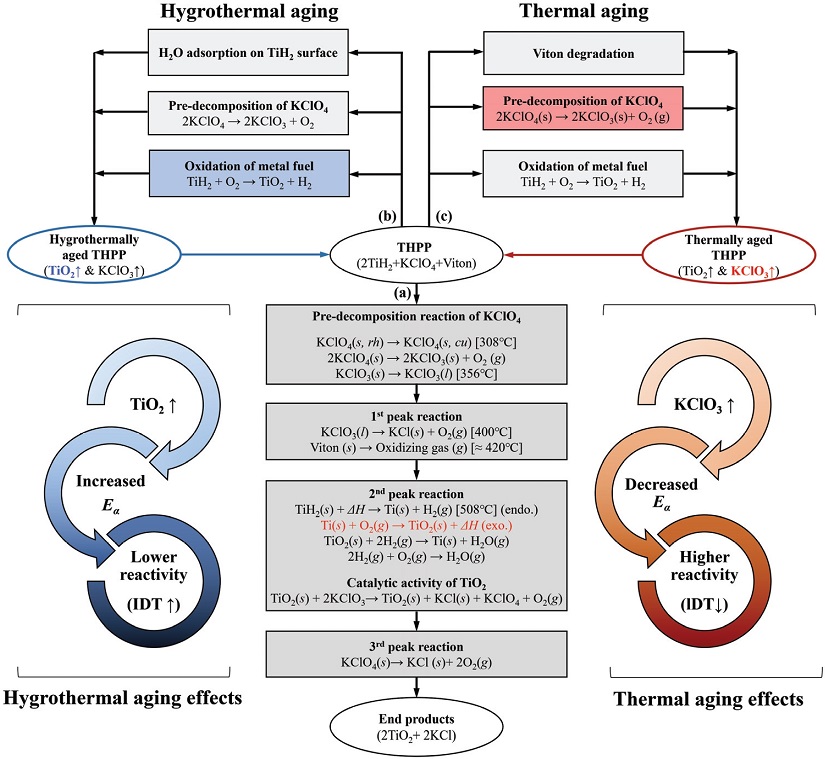
최종적으로 FE-SEM-EDS, 열분석 및 점화 실험을 이용하여 THPP의 노화에 따른 연소 및 점화 특성을 확인해본 결과 Fig. 13과 같이 나타낼 수 있다. 노화되지 않은 일반 THPP의 연소과정은 Fig. 13의 (a)의 경로와 같이 진행되지만, 열노화가 가해지면 경로 (c)와 같이 Viton의 열화와 연료의 산화, 산화제 분해 현상이 복합적으로 나타나게 되며 특히 산화제 분해 현상이 주된 반응으로 작용하게 된다. 이는 시료 내에 전체적으로 KClO3 함량의 증가를 초래하며, 뒤이어 활성화 에너지 감소 및 연소 지연시간과 연소시간의 감소로 이어지게 된다. 따라서 전체적으로 열노화의 반응성은 증가하지만 열 성능은 약화되어 제 성능을 발휘하지 못하게 될 것이다. 수분노화의 경우 경로(b)와 같이 시료 표면의 수증기 흡착과 더불어 산화제 분해, 연료 산화 반응이 발생하게 된다. 이때, 수분노화는 연료 산화 반응이 주된 반응으로 성능 파라미터에 영향을 미치게 된다. 이미 산화되어버린 연료로 인하여 활성화 에너지는 증가하고, 연소 반응의 둔감화로 이어지게 되어 본래 성능 발현(기대수명 10년, 열 성능 99% 보장[23])에 치명적인 영향을 미칠 것으로 판단된다.
4. 결 론
본 연구에서는 THPP 파이로 물질에 대하여 노화 조건 중 상대습도 변인을 달리하여 수분노화 메커니즘을 구축할 수 있었다. 일반적으로 금속 물질로 이루어진 연료와 KClO4와 같은 고형 종류의 산화제를 구성으로 하는 파이로 물질의 경우 대표적인 노화 효과로 ‘금속의 산화’와 ‘산화제의 분해’가 나타났다. 금속의 산화 즉, TiO2함량 증가와 더불어 KClO4로부터 분해되어 나온 생성물인 KClO3로 인하여 중요한 화학반응 인자인 활성화 에너지와 핵심적인 점화 특성인 점화지연시간의 변화를 이끌어내는 것을 확인해볼 수 있었다.
이때, KClO3 함량이 증가한 열노화 시료의 경우 반응성이 높은 특성으로 인하여 TiO2 효과를 상쇄시킬 만큼 단축된 연소 지연시간의 결과를 가져왔고, 높은 상대습도로 인하여 연료 산화가 급격하게 증가한 수분노화 시료의 경우 반응성이 둔감된 결과를 확인해볼 수 있었다. 이러한 결과를 토대로 추후 연구에서는 파이로 물질에 노화가 가해졌을 때, 금속 종류 및 수분함량에 따른 산화제 분해율 및 연료 산화율을 파악하여 더욱 자세하고 명확한 반응성 변화 모델을 구축할 수 있을 것이다. 나아가 노화에 견고한 특성을 가진 연료 종류의 파악 및 개발이 가능할 것이라 기대되는 바이다. 그뿐만 아니라, 노화 기간에 따른 금속의 산화율 변화를 측정하여 파이로 물질의 노화 특성 및 수명 예측/평가에 대한 발전 또한 가져올 수 있을 것이다.
Acknowledgments
[이 논문은 한국추진공학회 2020년도 추계학술대회(2020. 11. 25-27), 파라다이스호텔 부산) 발표논문을 심사하여 수정ㆍ보완한 것임.]
본 논문은 정부(과학기술정보통신부)의 재원으로 한국연구재단의 지원을 받아 수행된 연구입니다(NRF-2020R1F1A1072007).
References
- Verga, A. and Paravan, C., “A Comparative Study of the Aging Behavior of Different Nano-Sized Aluminum Powders,” In 8th European Conference for Aerospace Sciences (EUCASS 2019), Madrid, Spain, EUCASS 1-8, Jul. 2019.
-
Oh, J., Ambekar, A. and Yoh, J.J., “The hygrothermal aging effects of titanium hydride potassium perchlorate for pyrotechnic combustion,” Thermochimica Acta, Vol. 665, No. 13, pp. 102-110, 2018.
[https://doi.org/10.1016/j.tca.2018.05.019]

-
Yetter, R.A., Risha, G.A. and Son, S.F., “Metal particle combustion and nanotechnology,” Proceedings of the Combustion Institute, Vol. 32, No. 2, pp. 1819-1838, 2009.
[https://doi.org/10.1016/j.proci.2008.08.013]

-
Oh, J., Jang, S.G. and Yoh, J.J., “Towards understanding the effects of heat and humidity on ageing of a NASA standard pyrotechnic igniter,” Scientific Reports, Vol. 9, No. 1, pp. 1-12, 2019.
[https://doi.org/10.1038/s41598-019-46608-8]

-
Harisivasri, P.K., Sivapirakasam, S.P., Soni, P., Surianarayanan, M. and Balasubramanian, K.R., “Thermal reaction studies and prediction of stoichiometry of pyrotechnic compositions using DSC and XRD methods,” Thermochimica Acta, Vol. 675, No. 13, pp. 100-106, 2019.
[https://doi.org/10.1016/j.tca.2019.03.009]

-
Ulas, A. and Kuo, K.K., “Effect of aging on ignition delay times of a composite solid propellant under CO2 laser heating,” Combustion Science and Technology, Vol. 127, No. 1-6, pp. 319-331, 1997.
[https://doi.org/10.1080/00102209708935699]

-
Sanborn, W., Boyd, D., Sorensen, D. and Quebral, A., “The Accelerated Aging of the Pyrotechnic Materials THPP and ZPP,” In 44th AIAA/ASME/SAE/ASEE Joint Propulsion Conference & Exhibit, Hartford, CT, U.S.A., AIAA 2008-4720, Jul. 2008.
[https://doi.org/10.2514/6.2008-4720]

-
Sorensen, D.N., Quebral, A.P., Baroody, E.E. and Sanborn, W.B., “Investigation of the thermal degradation of the aged pyrotechnic titanium hydride/potassium perchlorate,” Journal of Thermal Analysis and Calorimetry, Vol. 85, No. 1, pp. 151-156, 2006.
[https://doi.org/10.1007/s10973-005-7365-5]

-
Sinha, S., Piekiel, N.W., Smith, G.L. and Morris, C.J., “Investigating aging effects for porous silicon energetic materials,” Combustion and Flame, Vol. 181, No. 14, pp. 164-171, 2017.
[https://doi.org/10.1016/j.combustflame.2017.03.015]

-
Ryu, J.H., Yang, J.H. and Yoh, J.J., “Novel utilization of the molecular band signal in metal oxides: understanding the aging process of pyrotechnic substances by using laser induced plasma emissions,” Optical Materials Express, Vol. 9, No. 2, pp. 410-422, 2019.
[https://doi.org/10.1364/OME.9.000410]

-
Thomas, J.C., Sammet, T.E., Dillier, C.A.M., Demko, A.R., Rodriguez, F.A. and Petersen, E.L., “Aging effects on the burning rates of composite solid propellants with nano-additives,” Journal of Propulsion and Power, Vol. 35, No. 2, pp. 342-351, 2019.
[https://doi.org/10.2514/1.B37189]

-
Kadiresh, P. and Sridhar, B.T.N., “Experimental study on ballistic behaviour of an aluminised AP/HTPB propellant during accelerated aging,” Journal of Thermal Analysis and Calorimetry, Vol. 100, No. 1, pp. 331-335, 2010.
[https://doi.org/10.1007/s10973-009-0569-3]

- Hohmann, C., “Propellant for the NASA standard initiator. National Aeronautics and Space Administration,” Lyndon B. Johnson Space Center, 2000.
-
Vyazovkin, S., Burnham, A.K., Criado, J.M., Pérez-Maqueda, L.A., Popescu, C. and Sbirrazzuoli, N., “ICTAC Kinetics Committee recommendations for performing kinetic computations on thermal analysis data,” Thermochimica Acta, Vol. 520, No. 1-2, pp. 1-19, 2011.
[https://doi.org/10.1016/j.tca.2011.03.034]

-
Friedman, H.L., “Kinetics of thermal degradation of char‐forming plastics from thermogravimetry. Application to a phenolic plastic,” In Journal of Polymer Science Part C: Polymer Symposia, Vol. 6, No. 1, pp. 183-195, 1964.
[https://doi.org/10.1002/polc.5070060121]

-
Jian, G., Chowdhury, S., Sullivan, K. and Zachariah, M.R., “Nanothermite reactions: Is gas phase oxygen generation from the oxygen carrier an essential prerequisite to ignition?,” Combustion and Flame, Vol. 160, No. 2, pp. 432-437, 2013.
[https://doi.org/10.1016/j.combustflame.2012.09.009]

-
Ryu, J.H., Yang, J.H. and Yoh, J.J., “A non-calorimetric approach for investigating the moisture-induced ageing of a pyrotechnic delay material using spectroscopies,” Scientific Reports, Vol. 9, No. 1, pp. 1-10, 2019.
[https://doi.org/10.1038/s41598-019-51667-y]

-
Lu, K.T. and Yang, C.C., “Thermal Analysis Studies on the Slow‐Propagation Tungsten Type Delay Composition System,” Propellants, Explosives, Pyrotechnics, Vol. 33, No. 5, pp. 403-410, 2008.
[https://doi.org/10.1002/prep.200700287]

-
Bhosle, V., Baburaj, E.G., Miranova, M. and Salama, K., “Dehydrogenation of TiH2,” Materials Science and Engineering: A, Vol. 356, No. 1-2, pp. 190-199, 2003.
[https://doi.org/10.1016/S0921-5093(03)00117-5]

-
Chen, K.S., “A simplified model of TiH1. 65/KClO4 pyrotechnic ignition,” No. SAND2009-1217, Sandia National Laboratories, 2009.
[https://doi.org/10.2172/959109]

-
Massis, T.M., “The processing, properties and use of the pyrotechnic mixture-titanium subhydride/potassium perchlorate,” In 32nd Joint Propulsion Conference and Exhibit, Lake Buena Vista, FL, U.S.A., AIAA-96-3019, Jul. 1996.
[https://doi.org/10.2514/6.1996-3019]

-
Park, K.B., Choi, J., Na, T.W., Kang, J.W., Park, K. and Park, H.K., “Oxygen Reduction Behavior of HDH TiH2 Powder during Dehydrogenation Reaction,” Metals, Vol. 9, No. 11, pp. 1154, 2019.
[https://doi.org/10.3390/met9111154]

- Conley, P.L., “Space vehicle mechanisms: elements of successful design,” John Wiley & Sons.New York: Wiley Subscription Services, Inc., A Wiley Company, 1964.